题目内容
【题目】已知: ①P4(S,白磷)+5O2(g)= P4O10(S)△H = —2983.2kJmol-1
②P(S,红磷)+5/4O2(g)=1/4P4O10(s) △H = —738.5kJmol-1
(1)写出白磷转化为红磷的热化学方程式:___________________________________。
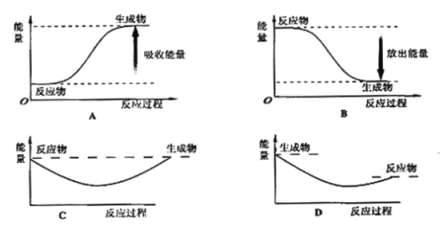
(2)则对应下列化学反应过程中的能量变化图,能正确反映出由白磷转化为红磷的是[选填A~D]________。
【答案】P4(s,白磷)= 4P(s,红磷) △H = —29.2kJmol-1B
【解析】
(1)由盖斯定律可知:将①-4②可得白磷转化为红磷的热化学方程式P4(s、白磷)=4P(s、红磷)△H=﹣2983.2kJ/mol+4×738.5kJmol﹣1=﹣29.2KJ/mol,故答案为:P4(s,白磷)= 4P(s,红磷) △H = —29.2kJmol-1;
(2)白磷转化为红磷是放热的反应,所以反应物的能量高于生成物的能量,B图符合此关系,故答案为:B。

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
【题目】下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
| ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ② | ③ | Ne | ||||||
3 | Na | ④ | ⑤ | ⑥ | |||||
(1)④的原子序数是________;
(2)⑤的原子结构示意图是____________;
(3)②和③两种元素的非金属性强弱关系是:②______③(填“>”、“<”或“=”);
(4)①和⑥两种元素组成的化合物中含有的化学键是____(填“共价”或“离子”)键。