题目内容
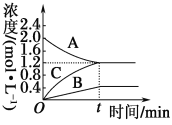
【题目】下图表示800℃时A、B、C三种气体物质的浓度随时间变化的情况。t是到达平衡状态的时间。试回答:
(1)该反应的反应物是________。
(2)该反应的化学反应方程式为_______________________________。
(3)若达到平衡状态的时间是2 min,A物质的平均反应速率为__________________。
【答案】A2A![]() B+3C 0.4 mol·L-1·min-1
B+3C 0.4 mol·L-1·min-1
【解析】
(1)由图可知,随着反应的进行,A的浓度降低,A为反应物,B、C的浓度增大,故B、C为生成物.故答案为:A;
(2)由图可知,△c(A)=2.0mol/L-1.2mol/L=0.8mol/L,△c(B)=0.4mol/L,△c(C)=1.2mol/L,A、B、C化学计量数之比等于浓度变化量之比为0.8mol/L∶0.4mol/L∶1.2mol/L=2∶1∶3,反应为可逆反应,故反应方程式为2AB+3C.故答案为:2AB+3C;
(3)由图可知△c(A)=2.0mol/L-1.2mol/L=0.8mol/L,所v(A)=![]() =0.4mol/(Lmin),故答案为:0.4mol/(Lmin)。
=0.4mol/(Lmin),故答案为:0.4mol/(Lmin)。

练习册系列答案
相关题目