��Ŀ����
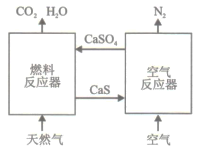
����Ŀ��N2O��CO�ǻ�����Ⱦ�����壬����Pt2O+����ת��Ϊ�����壬�䷴ӦΪN2O(g)+CO(g) CO2(g)+N2(g) ��H���йػ�ѧ��Ӧ�����ʱ仯����(ͼ1)�������仯����(ͼ2)���£�

����˵����ȷ����( )
A����ͼ1��֪����H1=��H+��H2
B����ͼ2��֪��H =-226 kJ/mol
C��Ϊ��ʵ��ת���費����Ӧ���в���Pt2O+��Pt2O2+
D����ͼ2��֪�÷�Ӧ����Ӧ�Ļ�ܴ����淴Ӧ�Ļ��
���𰸡�B
��������
���������A����N2O+Pt2O+ =Pt2O2+ +N2 ��H1����Pt2O2+ +CO= Pt2O+ +CO2 ��H2 ����ϸ�˹���ɼ����+�ڵõ�N2O(g)+CO(g)=CO2(g)+N2(g) ��H=��H1+��H2 ������B��ͼ2������֪����Ӧ�����������������ӦΪ���ȷ�Ӧ����Ӧ�ʱ��H=����������-��Ӧ������=134kJ/mol-360kJ/mol=-226kJ/mol����ȷ��C����N2O+Pt2O+ =Pt2O2+ +N2��H1����Pt2O2+ +CO= Pt2O+ +CO2 ��H2����Ӧ������Pt2O+��Pt2O2+���뷴Ӧ�������ɲ���Ҫ���䣬����D������Ӧ��Ӧ���E1=134KJ/molС���淴Ӧ���E2 =360KJ/mol������

����Ŀ���±�ΪԪ�����ڱ���ͬ�ڵ�һ���֣� A��B��C��D��E����Ԫ�������ڱ��е�λ������ͼ��ʾ��CԪ�ص�ԭ������������Ϊ������3����
A | E | C | |
B | D |
�ش��������⣺
��1��BԪ�������ڱ��е�λ��Ϊ__________��
��2��D������������Ӧˮ����Ļ�ѧʽΪ__________��
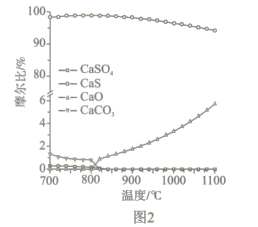
��3��������ʵ��˵��CԪ�صķǽ����Ա���Ԫ�صķǽ�����ǿ����__________��
a��C������H2S��Һ��Ӧ����Һ�����
b����������ԭ��Ӧ�У�1molC���ʱ�1molS�õ��Ӷ�
c��C��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
d. CԪ�صļ��⻯��е����SԪ�صļ��⻯��
��4��B��D��Ԫ�صĵ��ʷ�Ӧ���ɻ�����M�����Ľṹ���Ƽ��飬д��M�ĵ���ʽ_____��
��5��A��þ�γɵ�1mol������N��ˮ��Ӧ������2molMg(OH)2��1mol��̬��������������̼��������Ϊ9:1��д��N��ˮ��Ӧ�Ļ�ѧ����ʽ______________________________��
��6��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���ɵ�����������ɱ�������Ԫ����ɣ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ������Σ�����1L2.2mol/LNaOH��Һ��1molO2������������ķ���ʽ�����ʵ����ֱ�Ϊ__________��
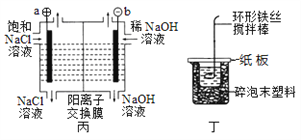
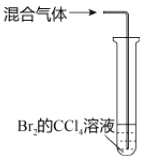
����Ŀ������ʵ�鷽���У��ܴﵽ��Ӧʵ��Ŀ�ĵ���
ʵ�鷽�� |
|
|
|
|
Ŀ�� | A���Ƚ��Ҵ��������ǻ���ԭ�Ӻ�ˮ��������ԭ�ӵĻ����� | B����ȥ��ϩ�еĶ������� | C����������Һ | D��֤��̼������ǿ�ڱ��� |
A. A B. B C. C D. D