题目内容
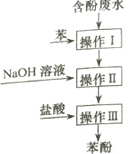
【题目】某同学设计了如下实验方法分离KNO3和Ba(NO3)2两种固体混合物并测定其含量:

(1)操作①的名称是____________,试剂a是____________(填化学式)。
(2)加入K2CO3溶液所发生反应的离子方程式是__________。
(3)按此实验方案分离得到的KNO3,经分析含有杂质K2CO3,除去K2CO3的操作为___________
(4)过滤后洗涤沉淀B的实验操作为________________。
(5)实验前称量混合物A的质量为m g,称量经洗涤干燥后的沉淀B的质量为w g,则混合物中Ba(NO3)2质量分数为______________________。
【答案】溶解 HNO3 CO32-+ Ba2+=BaCO3↓ 向滤液中再加入稀硝酸,待无气泡生成后,再蒸发结晶 将沉淀置于过滤器中,加水至刚好浸没沉淀,待水自然流下,再重复操作2~3次 ![]() ×100%
×100%
【解析】
向含有KNO3和Ba(NO3)2两种固体混合物中加入H2O,溶解,然后向所得溶液中加入过量K2CO3溶液,发生反应:K2CO3+Ba(NO3)2=BaCO3↓+2KNO3,过滤得沉淀B是BaCO3;
向沉淀B中加入过量稀硝酸,发生反应BaCO3+2HNO3=Ba(NO3)2+H2O+CO2↑,得到的溶液C中含Ba(NO3)2、HNO3,加热蒸发,HNO3挥发,最后得到的固体物质为Ba(NO3)2。
(1)操作①的名称是溶解,试剂a是HNO3。
(2)加入K2CO3溶液,发生反应:K2CO3+Ba(NO3)2=BaCO3↓+2KNO3,该反应的离子方程式是CO32-+ Ba2+=BaCO3↓。
(3)向含有KNO3和Ba(NO3)2混合溶液中加入过量的K2CO3,发生反应:K2CO3+Ba(NO3)2=BaCO3↓+2KNO3,得到的滤液中含有KNO3和过量的K2CO3,除去K2CO3的操作为向滤液中再加入稀硝酸待无气泡生成,然后再蒸发结晶;
(4)过滤后洗涤沉淀B的实验操作为将沉淀置于过滤器中,加水至刚好浸没沉淀,待水自然流下,再重复操作2~3次。
(5)沉淀B是BaCO3,沉淀B的质量为w g,则根据Ba元素守恒,可知Ba(NO3)2的质量为m[Ba(NO3)2]=![]() mol×261g/mol=
mol×261g/mol=![]() g,由于实验前称量混合物A的质量为m g,则混合物中Ba(NO3)2质量分数为
g,由于实验前称量混合物A的质量为m g,则混合物中Ba(NO3)2质量分数为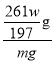 ×100%=
×100%=![]() ×100%。
×100%。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:

回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。

(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式______。