题目内容
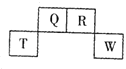
【题目】如图为元素周期表中短周期的一部分,四种元素中只有一种是金属,下列说法错误的是( )
A.气态氢化物稳定性:R>Q
B.元素T的离子半径>元素R的离子半径
C.与W同主族的某元素形成的18电子的氢化物分子中既有极性键又有非极性键
D.Q可形成多种同分异构体
【答案】B
【解析】
这几种元素都是短周期元素,根据元素在周期表中的位置知,T和W位于第三周期、Q和R位于第二周期,这几种元素只有一种金属,则T为金属,为Al,则Q、R、W分别是C、N、S元素;
A.元素的非金属性越强,其氢化物的稳定性越强,非金属性![]() ,所以氢化物的稳定性
,所以氢化物的稳定性![]() ,故A正确;
,故A正确;
B.电子层结构相同的离子,离子半径随着原子序数增大而减小,这两种离子电子层结构相同,原子序数![]() ,所以离子半径
,所以离子半径![]() ,故B错误;
,故B错误;
C.与W同主族的某元素形成的18电子的氢化物为![]() ,
,![]() 原子之间存在极性键、
原子之间存在极性键、![]() 原子之间存在非极性键,所以双氧水分子中存在极性键和非极性键,故C正确;
原子之间存在非极性键,所以双氧水分子中存在极性键和非极性键,故C正确;
D.碳单质有多种同素异形体,如:金刚石、石墨和![]() ,故D正确;
,故D正确;
故选B。

 阅读快车系列答案
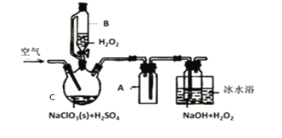
阅读快车系列答案【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯:

密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
已知: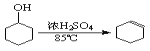 +H2O
+H2O
(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是__,导管B除了导气外还具有的作用是__。
②试管C置于冰水浴中的目的是__。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在__层(填“上”或“下”),分液后用__(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
②如再将环己烯进行蒸馏,冷却水应从__口进入(填“上”或“下”)。