题目内容
【题目】为验证Cl2、Br2的氧化性强弱,设计了如下实验: 
(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)
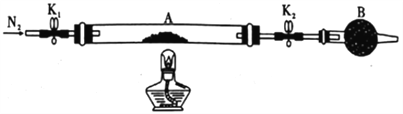
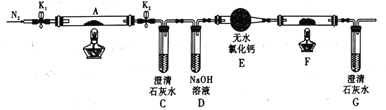
实验步骤如上图,填写图中的空白.
(1)2mL试剂为;加入少量试剂;再加入试剂;
(2)现象: .
(3)可以证明Cl2的氧化性(填“强于”或“弱于”)Br2的氧化性,此反应的离子方程式为: .
【答案】
(1)NaBr溶液;氯水;四氯化碳
(2)溶液分层,下层橙红色,上层无色
(3)强于;Cl2+2Br﹣=Br2+2Cl﹣
【解析】解:(1)要想比较氯气和溴单质的氧化性大小,做如下实验:
少量溴化钠反应→加适量氯水(振荡,溶液由黄绿色变成橙色)→加入四氯化碳(振荡)→现象(溶液分层,下层橙红色,上层无色)→说明氯气和溴离子反应,能证明氯气的氧化性大于溴.
故答案为:NaBr溶液;氯水;四氯化碳;(2)溴单质在四氯化碳中的溶解度大于在水中的溶解度,水和四氯化碳是互不相溶的,所以会看到:溶液分层,下层橙红色,上层无色;故答案为:液分层,下层橙红色,上层无色;(3)通过以上实验知,氯气能将溴单质置换出来,氯气的氧化性大于溴,离子方程式为:Cl2+2Br﹣=Br2+2Cl﹣ .
故答案为:强于;Cl2+2Br﹣=Br2+2Cl﹣ .
根据同一氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性来设计实验,要想比较氯气的氧化性大于溴的氧化性,只要使氯气和溴的盐溶液混合观察是否有溴单质生成,如果有溴单质生成就说明氯气的氧化性大于溴单质,否则不能证明.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目