题目内容
17.若某池(电解池或原电池)的总反应离子反应式是Cu+Zn2+═Cu2++Zn,关于此电池的有关说法正确的是( )| A. | 该池可能是原电池,也可能是电解池 | |
| B. | 该池只能是原电池,且电解质溶液为硝酸 | |
| C. | 该池只能是电解池,且金属铜为该电解池的阴极 | |
| D. | 该池只能是电解池,电解质溶液可以是硫酸锌 |
分析 根据电池反应式的反应物和生成物特点确定是原电池还是电解池,再根据得失电子确定电极材料,注意铜和锌离子不反应,据此分析.
解答 解:铜和锌离子不能自发的进行氧化还原反应,所以该反应只能是电解池反应而不是原电池反应,所以该装置只能构成电解池不能构成原电池;
该电解池中,阳极上铜失电子发生氧化反应,阴极上锌离子得电子发生还原反应,所以该电解池的阳极必须是铜电极,电解质溶液可以是硫酸锌,
故选D.
点评 本题考查了原电池和电解池原理,注意不能自发进行的氧化还原反应不能设计成原电池,为易错点.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
7.在硫酸钠和硫酸铝的混和溶液中,Al3+的物质的量浓度为0.2mol/L,SO42-为0.4mol/L,溶液中Na+的物质的量浓度为( )
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
5.己烯雌酚是一种激素类药物,结构如下,下列有关叙述中不正确的是( )

| A. | 可以用有机溶剂萃取 | |
| B. | 可与NaOH和NaHCO3发生反应 | |
| C. | 1mol该有机物可以与5mol Br2发生反应 | |
| D. | 该有机物分子中,可能有16个碳原子共平面 |
12.下列说法正确的是( )
| A. | 常温下,反应2A (s)+B (g)═2C (g)+D (g)不能自发进行,则该反应△H一定大于0 | |
| B. | 101kPa时,2 H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1,则H2的燃烧热为571.6kJ•mol-1 | |
| C. | C (石墨,s)═C (金刚石,s)△H1=+1.9kJ•mol-1,则由石墨制取金刚石的吸热反应,金刚石比石墨稳定 | |
| D. | 0.5molH2SO4与0.5mol Ba(OH)2完全反应所放出的热量即为中和热 |
2.为完成相应实验,实验器材(规格和数量不限)足够的一项是( )
| 相应实验 | 实验器材(省略夹持装置) | |
| A | 氯化钠溶液的浓缩结晶 | 烧杯、玻璃棒、酒精灯 |
| B | 用盐酸除去硫酸钡中的少量碳酸铜 | 烧杯、漏斗、胶头滴管、滤纸 |
| C | 用浓硫酸配制0.5mol•L-1的溶液 | 烧杯、玻璃棒、胶头滴管、容量瓶 |
| D | 用溴水和CCl4除去NaBr溶液中的少量NaI | 烧杯、玻璃棒、胶头滴管、分液漏斗 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关化学用语表示正确的是( )
| A. | Al3+的结构示意图: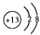 | B. | 水的电子式: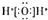 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 含有7个中子的碳原子:${\;}_{6}^{7}$C |
6.反应A+3B═4C+2D,在不同条件下反应,其平均反应速率v(X)(表示反应物的消耗速率或生成物的生成速率)如下,其中反应速率最快的是( )
| A. | v(A)=0.4mol/(L•s) | B. | v(B)=0.8mol/(L•s) | C. | v(C)=1.2mol/(L•s) | D. | v(D)=0.7mol/(L•s) |
7.现有1L 0.5mol/L的硫酸钠溶液,有关溶液的叙述正确的是( )
| A. | 取0.5 L溶液,Na+的浓度是0.5 mol/L | |
| B. | 取0.1 L溶液稀释至l L,SO42-离子浓度是0.05 mol/L | |
| C. | 溶质的离子总数是6.02×1023个 | |
| D. | 该溶液是把0.5 mol Na2SO4溶于1 L水中配制而成的 |