题目内容
下表是实验室制备气体的有关内容:
(1)上表气体中:从制备过程看,必须选择合适的氧化剂才能实现的是________(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是________。
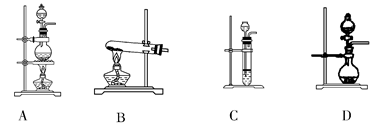
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。
(3)若用上述制备O2的装置制备NH3,则选择的试剂为________________。
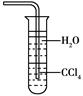
(4)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制。
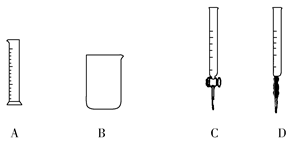
①为提高配制的精确度,量取浓盐酸的仪器可选用下列中的________(填序号):
②配制过程中,除上图所列仪器外,还需要的仪器有________、________、________。
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制氧气 | H2O2―→O2 | |
| ② | 制氨气 | NH4Cl―→NH3 | |
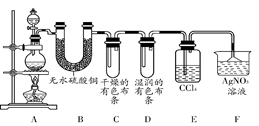
| ③ | 是氯气 | HCl―→Cl2 | |
(1)上表气体中:从制备过程看,必须选择合适的氧化剂才能实现的是________(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是________。
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中。

(3)若用上述制备O2的装置制备NH3,则选择的试剂为________________。
(4)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制。
①为提高配制的精确度,量取浓盐酸的仪器可选用下列中的________(填序号):

②配制过程中,除上图所列仪器外,还需要的仪器有________、________、________。
(1)Cl2 NH3
(2)
(3)浓氨水和固体氢氧化钠(或生石灰等)
(4)①C ②100 mL容量瓶 胶头滴管 玻璃棒
(2)
| 编号 | 发生装置 |
| ① | D |
| ② | B |
| ③ | A或D |
(3)浓氨水和固体氢氧化钠(或生石灰等)
(4)①C ②100 mL容量瓶 胶头滴管 玻璃棒
由HCl制备Cl2需要加氧化剂才能实现,制氧气、氯气均为氧化还原反应,制氨气为复分解反应。A、B、C、D四套装置分别可以用来进行的反应为:固体(液体)+液体需要加热,固体+固体需要加热,块状固体+液体不需要加热,固体(液体)+液体不需要加热。要提高量取液体的精确度应该用滴定管,取盐酸应该用酸式滴定管。

练习册系列答案
相关题目