题目内容
【题目】近期发现,H2S是继NO、CO之后第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(1)在密闭容器中充入一定量的H2S,发生反应2H2S(g)![]() 2H2(g)+S2 (g) 如图为H2S的转化率与温度、压强的关系。
2H2(g)+S2 (g) 如图为H2S的转化率与温度、压强的关系。
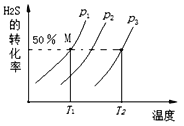
①该反应的ΔH__________0(填“>”、“=”或“<”);
②图中压强(p1、p2、p3)由小到大的顺序为_____________________;
③图中M点的平衡常数KP=_______________(KP是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)羰基硫(COS)是一种粮食熏蒸剂,能有效防止粮食被某些昆虫、线虫和真菌危害。在2 L的密闭容器中,保持温度T不变,将CO和H2S混合,并达下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g) K=0.2。开始投入9 molH2S和a mol CO,经10 min达到平衡。
COS(g)+H2(g) K=0.2。开始投入9 molH2S和a mol CO,经10 min达到平衡。
①若达平衡时n(H2S)=5mol,a 为_______。平衡时CO的转化率为________。
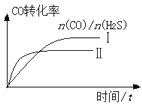
②曲线Ⅰ和Ⅱ表示该温度下,CO和H2S投料比[n(CO)/ n(H2S)]不同时,CO转化率随时间变化图像。则曲线Ⅰ和Ⅱ中a值的大小关系为:Ⅰ___Ⅱ(填“大于”“等于”“小于”),理由是____。
【答案】 > p1、p2、p3 1/5 p1 20 20% 小于 H2S的物质的量固定,投料比越大(即a值越大),CO转化率越低,但反应速率越快,达平衡时间越短
【解析】(1)①根据图像,升高温度,H2S的转化率增大,平衡正向移动,因此正反应为吸热反应,ΔH>0,故答案为:>;
②2H2S(g)2H2(g)+S2(g)△H>0,是气体体积增大的反应,温度不变,压强增大,平衡逆向移动,H2S的转化率减小,则压强关系为:p1<p2<p3,故答案为:p1<p2<p3;
③M点的H2S转化率为50%,总压为p1,设H2S起始量为2mol,
2H2S(g)2H2(g)+S2(g)
起始量(mol) 2 0 0
变化量(mol) 1 1 0.5
平衡量(mol) 1 1 0.5
平衡分压 ![]() p1
p1 ![]() p1
p1 ![]() p1
p1
Kp=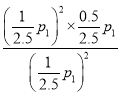 =
=![]() p1,故答案为:
p1,故答案为: ![]() p1;
p1;
(2)① CO(g)+H2S(g)![]() COS(g)+H2(g)
COS(g)+H2(g)
开始(mol/L) ![]() 4.5 0 0
4.5 0 0
反应(mol/L) 2 2 2 2
平衡(mol/L) ![]() -2 2.5 2 2
-2 2.5 2 2
K=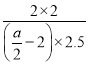 =0.2,解得:a=20,平衡时CO的转化率=
=0.2,解得:a=20,平衡时CO的转化率=![]() ×100%=20%,故答案为:20;20%;
×100%=20%,故答案为:20;20%;
②根据曲线Ⅰ和Ⅱ表示该温度下,CO和H2S投料比[n(CO)/ n(H2S)]不同时,CO转化率随时间变化图像,H2S的物质的量固定,投料比越大(即a值越大),CO转化率越低,但反应速率越快,达平衡时间越短,则曲线Ⅰ中a值小于曲线Ⅱ中a值,故答案为:小于;H2S的物质的量固定,投料比越大(即a值越大),CO转化率越低,但反应速率越快,达平衡时间越短。

【题目】活性炭可处理大气污染物NO.T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
活性炭/mol | NO/mol | A/mol | B/mol | |
起始状态 | 2.030 | 0.100 | 0 | 0 |
2min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2min内,用NO表示该反应的平均速率v(NO)=molL﹣1min﹣1 .
(2)该反应的化学方程式是 .
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是 .
①v(NO):v(A):v(B)=2:1:1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
①a处通入的物质是 , 电极反应式为:;
②b处电极反应式为;
③电池工作时H+由极移向极(填正、负极).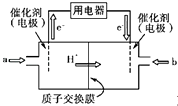
【题目】根据下列实验操作和现象,所得结论正确的是( )
实验操作 | 现象 | 结论 | |
A | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 该溶液中含有SO |
B | 将蘸有浓氨水的玻璃棒靠近蘸有某溶液的玻璃棒 | 有白烟产生 | 该溶液是浓盐酸 |
C | 将某气体通入品红溶液中 | 溶液红色褪去 | 该气体可能是SO2 |
D | 向某溶液中滴加稀NaOH溶液时,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 该溶液中不含NH |
A.A
B.B
C.C
D.D