题目内容
(12分)(1)下列每组中都有一种物质与其他物质在分类上不同,试分析每组中物质的组成规律,将这种不同于其他物质的物质找出来.
①NaCl、KCl、NaClO、BaCl2 ②浊液、溶液、胶体、水
(2)用98%的浓H2SO4(ρ=1.84 g/cm3)配制500 ml 0.5 mol/L的稀H2SO4,所需浓H2SO4的体积为________ml(小数点后保留一位有效数字),如果实验室有10 ml、20 ml、50 ml量筒,应选用 ml量筒,实验中还需要用到的仪器有 ,若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷却至室温即转移至容量瓶进行定容________②定容时仰视刻度线
③量取好浓硫酸倒入烧杯溶解后,用水洗涤量筒2-3次,将洗涤液倒入烧杯
(3)7.8g的镁铝合金与足量的稀盐酸反应,生成氢气的体积为8.96L(标准状况),则此反应中转移电子的个数为________________,由镁和铝分别产生的氢气的体积之比为________________
(4)取100ml的Na2CO3和Na2SO4的混合溶液与过量盐酸反应,生成0.896L(标况)CO2;若向原混合溶液中加入足量的Ba(OH)2溶液,得到沉淀的质量为10.21g,试计算混合溶液中Na2CO3的物质的量浓度是___________mol/L, Na2SO4的物质的量浓度是___________mol/L。
①NaCl、KCl、NaClO、BaCl2 ②浊液、溶液、胶体、水
(2)用98%的浓H2SO4(ρ=1.84 g/cm3)配制500 ml 0.5 mol/L的稀H2SO4,所需浓H2SO4的体积为________ml(小数点后保留一位有效数字),如果实验室有10 ml、20 ml、50 ml量筒,应选用 ml量筒,实验中还需要用到的仪器有 ,若实验中出现下列现象对所配溶液浓度有什么影响?(填偏高、偏低、无影响)
①浓硫酸溶解后未冷却至室温即转移至容量瓶进行定容________②定容时仰视刻度线
③量取好浓硫酸倒入烧杯溶解后,用水洗涤量筒2-3次,将洗涤液倒入烧杯
(3)7.8g的镁铝合金与足量的稀盐酸反应,生成氢气的体积为8.96L(标准状况),则此反应中转移电子的个数为________________,由镁和铝分别产生的氢气的体积之比为________________
(4)取100ml的Na2CO3和Na2SO4的混合溶液与过量盐酸反应,生成0.896L(标况)CO2;若向原混合溶液中加入足量的Ba(OH)2溶液,得到沉淀的质量为10.21g,试计算混合溶液中Na2CO3的物质的量浓度是___________mol/L, Na2SO4的物质的量浓度是___________mol/L。
(1)①NaClO ②水(2)13.6 mL ; 20; 烧杯、玻璃棒、胶头滴管、500 mL容量瓶
①偏高 ②偏低③偏高(3)4.816×1023 1∶3 (4)Na2CO3 0.4 mol/L Na2SO4 0.1 mol/L
①偏高 ②偏低③偏高(3)4.816×1023 1∶3 (4)Na2CO3 0.4 mol/L Na2SO4 0.1 mol/L
(1)①NaClO是含氧酸盐,其余都是无氧酸盐。
②水是纯净物,其余都是混合物。
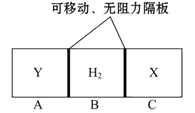
(2)500 ml 0.5 mol/L的稀H2SO4中溶质的物质的量是0.25mol,质量是24.5g。所以需要浓硫酸的体积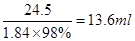 ;量取13.6ml浓硫酸,所需要量筒的规格应该大于13.6mol,且和13.6ml越接近,误差越小,所以选择20ml的量筒;配制一定物质的量浓度溶液的实验中需要的仪器是烧杯、玻璃棒、胶头滴管、500 mL容量瓶;根据c=n/V可知,①未冷却至室温即转移至容量瓶,则冷却后容量瓶中溶液的体积偏小,浓度偏高;②定容时仰视刻度线,则容量瓶中溶液的体积偏多,浓度偏小;③如果洗涤量筒并将洗涤液注入容量瓶中,则溶质的物质的量偏多,浓度偏高。
;量取13.6ml浓硫酸,所需要量筒的规格应该大于13.6mol,且和13.6ml越接近,误差越小,所以选择20ml的量筒;配制一定物质的量浓度溶液的实验中需要的仪器是烧杯、玻璃棒、胶头滴管、500 mL容量瓶;根据c=n/V可知,①未冷却至室温即转移至容量瓶,则冷却后容量瓶中溶液的体积偏小,浓度偏高;②定容时仰视刻度线,则容量瓶中溶液的体积偏多,浓度偏小;③如果洗涤量筒并将洗涤液注入容量瓶中,则溶质的物质的量偏多,浓度偏高。
(3)标准状况下8.96L氢气是0.4mol,转移电子是0.8mol,数目是0.8×6.02×1023 =4.816×1023 ;设镁和铝的物质的量分别是x、y,则24x+27y=7.8g、x+1.5y=0.4,解得x︰y=1∶3。
(4)0.896L(标况)CO2是0.04mol,所以根据碳原子守恒可知,碳酸钠是0.04mol,浓度是0.4mol/L;碳酸钠生成的白色沉淀是0.04mol,质量是7.88g,则硫酸钡的质量是2.33g,物质的量是0.01mol,所以硫酸钠的物质的量也是0.01mol,浓度是0.1mol/L。
②水是纯净物,其余都是混合物。
(2)500 ml 0.5 mol/L的稀H2SO4中溶质的物质的量是0.25mol,质量是24.5g。所以需要浓硫酸的体积
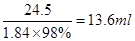 ;量取13.6ml浓硫酸,所需要量筒的规格应该大于13.6mol,且和13.6ml越接近,误差越小,所以选择20ml的量筒;配制一定物质的量浓度溶液的实验中需要的仪器是烧杯、玻璃棒、胶头滴管、500 mL容量瓶;根据c=n/V可知,①未冷却至室温即转移至容量瓶,则冷却后容量瓶中溶液的体积偏小,浓度偏高;②定容时仰视刻度线,则容量瓶中溶液的体积偏多,浓度偏小;③如果洗涤量筒并将洗涤液注入容量瓶中,则溶质的物质的量偏多,浓度偏高。
;量取13.6ml浓硫酸,所需要量筒的规格应该大于13.6mol,且和13.6ml越接近,误差越小,所以选择20ml的量筒;配制一定物质的量浓度溶液的实验中需要的仪器是烧杯、玻璃棒、胶头滴管、500 mL容量瓶;根据c=n/V可知,①未冷却至室温即转移至容量瓶,则冷却后容量瓶中溶液的体积偏小,浓度偏高;②定容时仰视刻度线,则容量瓶中溶液的体积偏多,浓度偏小;③如果洗涤量筒并将洗涤液注入容量瓶中,则溶质的物质的量偏多,浓度偏高。(3)标准状况下8.96L氢气是0.4mol,转移电子是0.8mol,数目是0.8×6.02×1023 =4.816×1023 ;设镁和铝的物质的量分别是x、y,则24x+27y=7.8g、x+1.5y=0.4,解得x︰y=1∶3。
(4)0.896L(标况)CO2是0.04mol,所以根据碳原子守恒可知,碳酸钠是0.04mol,浓度是0.4mol/L;碳酸钠生成的白色沉淀是0.04mol,质量是7.88g,则硫酸钡的质量是2.33g,物质的量是0.01mol,所以硫酸钠的物质的量也是0.01mol,浓度是0.1mol/L。

练习册系列答案
相关题目
 ? SO
? SO
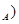 无关的组合是
无关的组合是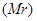 ②摩尔质量(M) ③原子半径(r) ④物质的量(n) ⑤气体摩尔体积(V
②摩尔质量(M) ③原子半径(r) ④物质的量(n) ⑤气体摩尔体积(V