题目内容
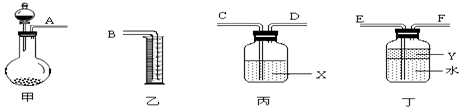
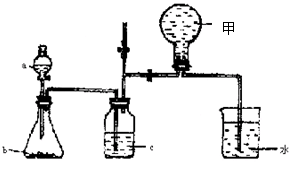
(共13分)(1)右图甲中装置甲是某种不溶于水的气体X的发生装置和收集装置(必要时可以加热),所用的试剂从下列试剂中选取2-3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀氨水、大理石、浓硫酸、浓硝酸、稀硝酸、蒸馏水。
回答下列问题:

①气体X的分子式是 。
②所选择的药品a是 ,b是 , c是 。
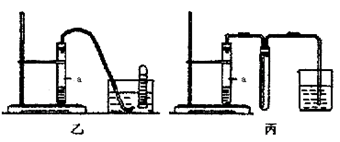
③下列装置乙和丙,能代替装置甲的简易装置是 (填“乙”或“丙”)
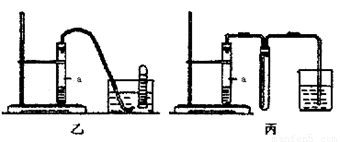
④请写出在试管a中所发生反应的化学方程式 。
⑤从反应开始到反应结束,预期在试管a中可观察到的气体的实验现象有哪些,请依次逐步写出 ; ;
(2)在进行研究性学习的过程中,学生发现等质量的铜片分别与等质量均过量的浓硝酸或稀硝酸反应,所得到溶液前者呈绿色,后者呈蓝色,针对这种现象,学生进行了讨论,出现两种意见,一种认为:Cu2+浓度差异引起了这种现象,你认为 (填“正确”或“不正确”),依据是: ;
另一种意见是:溶液呈绿色可能是Cu2+与NO2混合的结果,并用实验进行了证明,请简述实验方案与实验现象: 。
(1) ① NO ② a稀硝酸 b铜屑 c蒸馏水 ③ 乙
④3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
⑤试管a的溶液中有无色气泡产生;试管a上部空间气体由无色变成红棕色,又变无色;
(2)不正确 依据是:铜片质量相同,生成铜离子的物质的量相同,溶液体积相同且硝酸过量,故生成的Cu2+的浓度相同。
方案及实验现象:将绿色溶液加热,有红棕色气体产生,溶液变成蓝色,说明后一种推断正确。或:将溶液稀释,溶液变蓝色(其它合理方案均可)
【解析】

(共13分)〔一〕实验室用氢氧化钠配制1.00mol/L的氢氧化钠溶液0.2L,回答下列问题
(1)下列有关使用托盘天平的叙述,正确的是 。
A.称量前先调节天平的零点。
B.称量时左盘放被称量物,右盘放砝码。
C.氢氧化钠必须放在玻璃器皿里称量。
D.称量时,应先加质量小后加质量大的砝码至天平平衡。
E.称量完毕,应把天平放回砝码盒中。
(2)某同学用托盘天平称取一盛有氢氧化钠药品的烧杯,若左盘上放有30g砝码,游码位置如下图所示,天平的指针指在标尺的中间。则烧杯和粉剂的总质量为_________克。
〔二〕用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500ml的操作步骤如下:①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容、摇匀 ,请按要求填空:
(1)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。
(2)第⑤步实验的操作是(文字叙述)_______________________________________________
(3)某学生的下列操作中使浓度偏低的原因是: 。
① 用量筒量取浓硫酸时,俯视读数。
② 量筒中浓硫酸全部转入烧杯中稀释后,再转移到100ml容量瓶中,烧杯未洗涤。
③ 用玻璃棒引流,将溶液转移到容量瓶中有溶液流到了容量瓶外面。
④ 浓硫酸在小烧杯中稀释后,没有冷却就马上转移入容量瓶。
⑤ 用胶头滴管加蒸馏水时,加入过快而使液面超过了刻度线,立即用滴管吸去多余的水,使溶液凹石刚好与刻度线相切。
⑥ 滴加入蒸馏水,使溶液凹面刚好与刻度线相切,盖上瓶塞反复摇匀后,静置,发现液石比刻度线低,再加水至刻度线。