题目内容
在理论上可用来设计原电池的反应是
| A.Fe +2HCl =" Fe" Cl2+ H2 |
| B.NaOH +HCl="NaCl+" H2O |
| C.Cu SO4 +2NaOH= Cu(OH)2+Na2 SO4 |
| D.Ca CO3+2HCl=" Ca" Cl2+ H2O+ CO2 |
A
解析试题分析:常温能自发进行的氧化还原反应可设计成原电池,有元素化合价变化的反应为氧化还原反应,以此来解答。A中反应是置换反应,属于氧化还原反应,能用于设计原电池,A正确;B中反应是中和反应、C和D中都是复分解反应,反应中没有元素的化合价变化,不是氧化还原反应,因此不能用于设计原电池,故BCD均不符合题意,因此答案选A。
考点:考查原电池设计的有关判断
点评:该题是高考中的常见题型,属于基础性试题的考查,侧重对学生基础知识的巩固和训练。明确能自发进行的氧化还原反应能设计成原电池是解答本题的关键,准确判断出反应中有关元素的化合价变化是前提。

练习册系列答案
相关题目
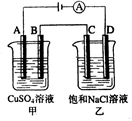
如图所示的装置,通电一段时间后,测得甲池中某电极质量增加2.16 g,乙池中某电极上析出0.64 g某金属,下列说法正确的是
| A.甲池b极上析出金属银,乙池c极上析出某金属 |
| B.甲池a极上析出金属银,乙池d极上析出某金属 |
| C.某盐溶液可能是CuSO4溶液 |
| D.某盐溶液可能是Mg(NO3)2溶液 |
某同体酸燃料电池以Ca(HSO )
)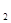 固体为电解质传递H
固体为电解质传递H ,其基本结构如图所示,电池总反应可表示为:2H
,其基本结构如图所示,电池总反应可表示为:2H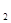 +O
+O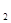 =2H
=2H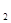 O,下列有关说法错误的是
O,下列有关说法错误的是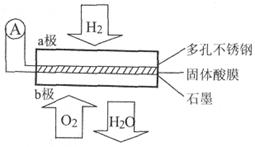
| A.电子通过外电路从a极流向b极 |
B.b极上的电极反应式为:O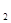 +4H +4H +4e +4e =2H =2H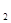 O O |
| C.每转移0.4 mol电子,生成3.6g水 |
D.H 由b极通过固体酸电解质传递到a极 由b极通过固体酸电解质传递到a极 |
下图是生活中常用的锌锰干电池的示意图,下列有关说法中不正确的是( ) 
| A.电池内部含有电解质 | B.锌是负极,碳棒是正极 |
| C.电池用完后可埋入土壤 | D.锌锰干电池属一次电池 |
将锌片和铜片用导线连接后放入硫酸铜溶液中,发生原电池反应(反应前后溶液体积不变),在反应过程中,下列叙述错误的是
| A.电子由锌片经导线流向铜片 | B.铜片作正极,锌片作负极 |
| C.溶液中SO42- 的物质的量浓度保持不变 | D.溶液中Cu2+移向负极 |
下图为铜锌原电池示意图,下列说法正确的是
| A.电子由铜片通过导线流向锌片 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.锌片逐渐溶解 |
| D.该装置能将电能转变为化学能 |
蓄电池放电时是起原电池的作用,在充电时起电解池的作用。下式是爱迪生蓄电池分别在充电、放电时的反应: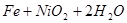

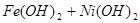 ,下列有关爱迪生电池的各种推断中错误的是( )。
,下列有关爱迪生电池的各种推断中错误的是( )。
A.放电时铁做负极, 做正极 做正极 |
B.充电时阴极上的电极反应为: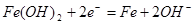 |
| C.放电时,电解质溶液中的阴离子是向正极方向移动 |
| D.蓄电池的两个电极必须浸入在碱性溶液中 |