题目内容
由一种阳离子与两种酸根离子组成的盐称为混盐.如CaOCl2是由Ca2+、Cl-、ClO-组成的混盐,在酸性条件下可以产生Cl2.下列有关判断不正确的是( )
| A、CaOCl2属于混合物 | B、CaOCl2的水溶液呈碱性 | C、CaOCl2具有较强的氧化性 | D、CaOCl2与硫酸反应转移1 mol电子时生成71 g Cl2 |
分析:CaOCl2是由Ca2+、Cl-、ClO-组成的混盐,在酸性条件下可以产生Cl2,反应方程式为:Cl-+ClO-+2H+=Cl2↑+H2O,根据氧化还原反应分析解答.
解答:解:A.CaOCl2只含一种物质,所以是纯净物,故A错误;
B.次氯酸钙是弱酸强碱盐,其水溶液呈碱性,故B正确;
C.Ca(ClO)2中Cl元素化合价为+1价,具有强氧化性,故C正确;
D.反应的离子方程式为Cl-+ClO-+2H+=Cl2+H2O,转移NA个电子时生成1mol氯气,其质量是71g,故D正确;
故选A.
B.次氯酸钙是弱酸强碱盐,其水溶液呈碱性,故B正确;
C.Ca(ClO)2中Cl元素化合价为+1价,具有强氧化性,故C正确;
D.反应的离子方程式为Cl-+ClO-+2H+=Cl2+H2O,转移NA个电子时生成1mol氯气,其质量是71g,故D正确;
故选A.
点评:本题考查氧化还原反应,题目难度不大,注意把握混盐的成分为解答该题的关键,学习中注意把握相关物质的性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程。我们目前中学课本中的酸碱理论是1887年阿仑尼乌斯(Arrhenius)提出了的电离理论。
(1)1905年富兰克林(Franklin)把阿仑尼乌斯以水为溶剂的个别现象,推到任何溶剂,提出了酸碱溶剂理论。溶剂理论认为:凡能离解而产生溶剂正离子的物质为酸,凡能离解而产生溶剂负离子的物质为碱。试写出五氯化磷在某条件下自身电离的方程式:
▲ (一种为正四面体阳离子,另一种为正八面体阴离子)。
(2)1923年丹麦化学家布朗斯物(Brφusted)和英国化学家劳莱(Lowry)提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列粒子在水溶液既可看作酸又可看作碱的是 ▲ 。
| A.HSO3- | B.NH4+ | C.OH- | D.HCO3- E.CH3COO- F.Cl- |
酸(电子对接受体) 碱(电子对给予体) 反应产物
H+ + [∶OH ]—
 H∶OH
H∶OH试指出下列两个反应中的酸或碱
①H3BO3 + H2O = H+ + B(OH)4- 该反应中的碱是 ▲ (填:H3BO3或 H2O)
②BF3 + NH3 = BF3· NH3 该反应中的酸是 ▲ (填:BF3 或 NH3)
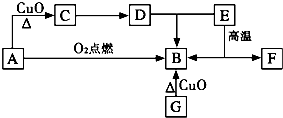 A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1:1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.?
A是生活中最常见的有机物,该化合物的蒸气对氢气的相对密度是23,是生物燃料之一.C的溶液能发生银镜反应,反应后的溶液经酸化可得D.G为单质,其原子最外层电子数为次外层的2倍.F中阴阳离子个数比为1:1,其阳离子与Ar具有相同的电子层结构,A-F的转化关系如图.? H∶OH
H∶OH