题目内容
为除去KCl溶液中的少量MgCl2、MgSO4,可选用以下三种试剂:氢氧化钡溶液、稀盐酸和碳酸钾溶液,按如图所示步骤进行操作:
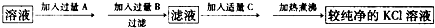
(1)写出三种试剂的化学式A
(2)根据上述步骤完成下列表格:
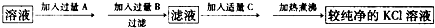
(1)写出三种试剂的化学式A
Ba(0H)2
Ba(0H)2
,BK2CO3
K2CO3
,CHCl
HCl
.(2)根据上述步骤完成下列表格:
| 目的 | 离子方程式 | |
| 加入过量A | ||
| 加入过量B | ||
| 加热煮沸 |
分析:由流程图可知,为除去KCl溶液中的少量MgCl2、MgSO4,A为Ba(0H)2,将镁离子、硫酸根离子转化为沉淀,再加B为K2CO3,将过量钡离子转化为沉淀,过滤后,向滤液中加适量C为稀盐酸,将过量的碳酸钾反应生成生成KCl,最后加热煮沸得到KCl溶液,以此来解答.
解答:解:由流程图可知,为除去KCl溶液中的少量MgCl2、MgSO4,A为Ba(0H)2,将镁离子、硫酸根离子转化为沉淀,再加B为K2CO3,将过量钡离子转化为沉淀,过滤后,向滤液中加适量C为稀盐酸,将过量的碳酸钾反应生成生成KCl,最后加热煮沸得到KCl溶液,以
(1)由上述分析可知,A为Ba(0H)2,B为K2CO3,C为HCl,故答案为:Ba(0H)2;K2CO3;HCl;
(2)由分析可知,A将镁离子、硫酸根离子转化为沉淀,发生Mg2++2OH-=Mg(OH)2↓、Mg2++SO42-+Ba2++2OH-=Mg(OH)2↓+BaSO4↓,B除去过量的钡离子,发生CO32-+Ba2+=BaCO3↓,加热煮沸除去过量的HCl,
故答案为:
(1)由上述分析可知,A为Ba(0H)2,B为K2CO3,C为HCl,故答案为:Ba(0H)2;K2CO3;HCl;
(2)由分析可知,A将镁离子、硫酸根离子转化为沉淀,发生Mg2++2OH-=Mg(OH)2↓、Mg2++SO42-+Ba2++2OH-=Mg(OH)2↓+BaSO4↓,B除去过量的钡离子,发生CO32-+Ba2+=BaCO3↓,加热煮沸除去过量的HCl,
故答案为:
| 除尽Mg2+和SO42- | Mg2++2OH-=Mg(OH)2↓ Mg2++SO42-+Ba2++2OH-=Mg(OH)2↓+BaSO4↓ |
| 除尽过量的Ba2+ | CO32-+Ba2+=BaCO3↓ |
| 除尽过量的HCl |
点评:本题考查物质的分离、提纯及除杂,把握流程中试剂的加入顺序及发生的离子反应为解答的关键,侧重除杂及离子反应的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
为除去KCl溶液中的少量MgCl2、MgSO4,可选用以下三种试剂:氢氧化钡溶液、稀盐酸和碳酸钾溶液,按下图所示步骤进行操作:
![]()
(1)写出三种试剂的化学式A ,B ,C 。
(2)根据上述步骤完成下列表格:
| 目的 | 离子方程式 | |
| 加入过量A | ||
| 加入过量B | ||
| 加热煮沸 |