题目内容
 合金在生产生活中的应用日趋广泛.
合金在生产生活中的应用日趋广泛.①镁合金被用于制笔记本电脑外壳、竞赛自行车车架等,是由于镁合金具有
②为测定某镁铝合金中镁的质量分数.称取一定质量的样品放入NaOH溶液中,发生反应的离子方程式是
③有一种镁铝合金(Mg17Al12)是贮氢材料,该合金在一定条件下吸氢的反应方程式为Mg17Al12+17H2=17MgH2+12Al.得到的混合物在6.0mol/LHCl溶液中能完全释放出H2.1mol Mg17A112完全吸氢后得到的混合物与上述盐酸完全反应,释放出H2的物质的量为
④铝电池性能优越.Al-空气燃料电池通常以NaCl溶液或KOH溶液为电解质溶液,通入空气的电极为正极,以多孔石墨为正极材料.若以NaCl溶液为电解质溶液,正极的反应武为
分析:①镁合金具有硬度大、密度小、散热性好、抗震性好等优点;
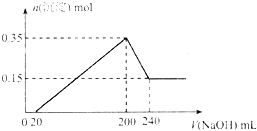
②Al与NaOH溶液反应,而Mg不能,由图可知,200mL~240mL发生Al(0H)3+NaOH=NaAlO2+2H2O,生成0.15molMg(OH)2和(0.35mol-0.15mol)Al(0H)3,结合原子守恒及反应计算;
③Mg17Al12+17H2=17MgH2+12Al,得到的混合物在6.0mol/LHCl溶液中能完全释放出H2,则Mg17Al12+70HCl=17MgCl2+12AlCl3+35H2↑,以此计算;
④Al-空气燃料电池以NaCl溶液为电解质溶液,正极上氧气得到电子;以KOH溶液为电解质溶液,电池反应为Al、氧气、KOH反应生成偏铝酸钾和水.
②Al与NaOH溶液反应,而Mg不能,由图可知,200mL~240mL发生Al(0H)3+NaOH=NaAlO2+2H2O,生成0.15molMg(OH)2和(0.35mol-0.15mol)Al(0H)3,结合原子守恒及反应计算;
③Mg17Al12+17H2=17MgH2+12Al,得到的混合物在6.0mol/LHCl溶液中能完全释放出H2,则Mg17Al12+70HCl=17MgCl2+12AlCl3+35H2↑,以此计算;
④Al-空气燃料电池以NaCl溶液为电解质溶液,正极上氧气得到电子;以KOH溶液为电解质溶液,电池反应为Al、氧气、KOH反应生成偏铝酸钾和水.
解答:解:①镁合金具有硬度大、密度小、散热性好、抗震性好等优点,故答案为:硬度大、密度小、散热性好、抗震性好;
②Al与NaOH溶液反应,而Mg不能,则合金溶于NaOH溶液发生的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,由图可知,生成0.15molMg(OH)2和(0.35mol-0.15mol)Al(0H)3,由Al原子守恒可知,n(Al)=0.2mol,其质量为0.2mol×27g/mol=5.4g,由200mL~240mL发生Al(0H)3+NaOH=NaAlO2+2H2O,消耗n(NaOH)=0.2mol,所以c(NaOH)=
=5mol/L,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;5.4;5;
③由Mg17Al12+17H2=17MgH2+12Al,得到的混合物在6.0mol/LHCl溶液中能完全释放出H2,则Mg17Al12+70HCl=17MgCl2+12AlCl3+35H2↑,
所以1mol Mg17A112完全吸氢后得到的混合物与上述盐酸完全反应,释放出H2的物质的量为35mol+17mol=52mol,
故答案为:52mol;
④Al-空气燃料电池以NaCl溶液为电解质溶液,正极上氧气得到电子,正极反应为O2+2H2O+4e-=4OH-;以KOH溶液为电解质溶液,电池反应为Al、氧气、KOH反应生成偏铝酸钾和水,该电池反应为4Al+3O2+4KOH=4KAlO2+2H2O,
故答案为:O2+2H2O+4e-=4OH-;4Al+3O2+4KOH=4KAlO2+2H2O.
②Al与NaOH溶液反应,而Mg不能,则合金溶于NaOH溶液发生的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑,由图可知,生成0.15molMg(OH)2和(0.35mol-0.15mol)Al(0H)3,由Al原子守恒可知,n(Al)=0.2mol,其质量为0.2mol×27g/mol=5.4g,由200mL~240mL发生Al(0H)3+NaOH=NaAlO2+2H2O,消耗n(NaOH)=0.2mol,所以c(NaOH)=
| 0.2mol |
| 0.04L |
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;5.4;5;
③由Mg17Al12+17H2=17MgH2+12Al,得到的混合物在6.0mol/LHCl溶液中能完全释放出H2,则Mg17Al12+70HCl=17MgCl2+12AlCl3+35H2↑,
所以1mol Mg17A112完全吸氢后得到的混合物与上述盐酸完全反应,释放出H2的物质的量为35mol+17mol=52mol,
故答案为:52mol;
④Al-空气燃料电池以NaCl溶液为电解质溶液,正极上氧气得到电子,正极反应为O2+2H2O+4e-=4OH-;以KOH溶液为电解质溶液,电池反应为Al、氧气、KOH反应生成偏铝酸钾和水,该电池反应为4Al+3O2+4KOH=4KAlO2+2H2O,
故答案为:O2+2H2O+4e-=4OH-;4Al+3O2+4KOH=4KAlO2+2H2O.
点评:本题考查较综合,涉及Al的化学性质、反应方程式及图象的计算及电化学,③为解答的易错点,注重高考高频考点的考查,较好的体现学生双基和计算能力、图象分析能力,题目难度中等.

练习册系列答案
相关题目

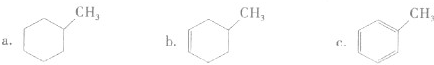
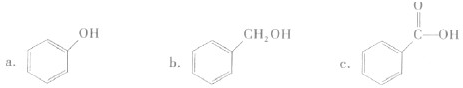
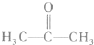



 和面心上的元素为 (填具体的元素符号)。
和面心上的元素为 (填具体的元素符号)。