题目内容
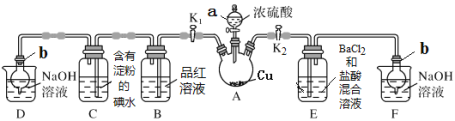
【题目】研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。

(1)仪器A的名称为________;A中反应的离子方程式为________。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为________。
②不能证明产生的气体中含有HCl的实验是________(填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:______________________________________。
(4)已知:2S2O32-+I2=== S4O62-+2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL-1 AgNO3溶液滴定所得溶液中的Cl-。
①X中的HClO不会影响I的测定结果,原因是________。
②由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 molL-1 AgNO3溶液的体积应大于________mL(用含V的代数式表示)。
【答案】圆底烧瓶MnO2 + 4H++ 2Cl- =Cl2↑+ 2H2O +Mn2+溶液先变红再褪色a、bCl2+ H2O![]() HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体答案一:生成1 mol HClO需消耗1 mol Cl2, HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2。答案二:Cl2+ H2O
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体答案一:生成1 mol HClO需消耗1 mol Cl2, HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2。答案二:Cl2+ H2O![]() HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应0.4V
HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应0.4V
【解析】
(1)该仪器没有支管,是圆底烧瓶;二氧化锰与浓盐酸加热反应生成氯化锰、氯气和水,离子方程式为:MnO2 + 4H++ 2Cl-![]() Cl2↑+ 2H2O +Mn2+ ;正确答案:圆底烧瓶;MnO2 + 4H++ 2Cl-
Cl2↑+ 2H2O +Mn2+ ;正确答案:圆底烧瓶;MnO2 + 4H++ 2Cl-![]() Cl2↑+ 2H2O +Mn2+。
Cl2↑+ 2H2O +Mn2+。
(2)①氯气和水反应生成盐酸和次氯酸,盐酸电离产生氢离子,溶液显酸性,紫色石蕊试剂显红色,次氯酸具有漂白性,使变红的溶液褪色,所以,看到的现象为先变红再褪色;正确答案:溶液先变红再褪色。
②由于氯气溶于水生成盐酸和次氯酸,盐酸电离出氢离子和氯离子,溶液显酸性,氯离子遇到银离子产生白色沉淀,所以ab都不能证明产生的气体中含有HCl;正确选项ab。
(3) Cl2+ H2O![]() HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,使氯化钠的沉淀溶解平衡右移,所以能析出氯化钠晶体;正确答案:Cl2+ H2O
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,使氯化钠的沉淀溶解平衡右移,所以能析出氯化钠晶体;正确答案:Cl2+ H2O![]() HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
(4)①HClO也有氧化性,1molHClO能将2molKI氧化成I2,生成1molHClO需消耗1molCl2,相当于也是1molCl2将2molKI氧化成I2;或者从平衡角度解释也可以,Cl2+ H2O![]() HCl+HClO,Cl2发生反应时,上述平衡逆向移动,最终盐酸和次氯酸都消耗完,相当于Cl2全部参与氧化I-的反应;正确答案:答案一:生成1molHClO需消耗1 molCl2, HClO也有氧化性,1mol HClO和1molCl2均能将2 molKI氧化成I2。答案二:Cl2+ H2O
HCl+HClO,Cl2发生反应时,上述平衡逆向移动,最终盐酸和次氯酸都消耗完,相当于Cl2全部参与氧化I-的反应;正确答案:答案一:生成1molHClO需消耗1 molCl2, HClO也有氧化性,1mol HClO和1molCl2均能将2 molKI氧化成I2。答案二:Cl2+ H2O![]() HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
②1mol氯气对应1mol碘,对应2mol硫代硫酸根离子,所以氯气的物质的量(0.04×V×10-3)/2=0.02V×10-3mol, 根据Cl2—2Cl---2AgCl---2Ag+关系可知,银离子的物质的量为0.04V×10-3mol,所以硝酸银溶液的体积V=n/c=0.4V×10-3L=0.4V mL;A中产生的气体若是含有氯化氢,氯化氢也会与硝酸银反应,所以消耗硝酸银溶液的体积应大于0.4V mL;正确答案:0.4V。