题目内容
20.将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( )
| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中铜片是正极,乙中铜片是负极 | ||
| C. | 两烧杯中溶液的pH均增大 | D. | 甲、乙溶液均变蓝色 |
分析 根据题给装置图知,甲为铜锌原电池,锌作负极,失电子,铜作正极,H+在铜电极上得电子,生成H2,总反应式为:Zn+H2SO4=ZnSO4+H2↑;乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑,以此进行分析.
解答 解:根据题给装置图知,甲为铜锌原电池,锌作负极,失电子,铜作正极,H+在铜电极上得电子,生成H2,总反应式为:Zn+H2SO4=ZnSO4+H2↑;乙装置中只是锌片与稀硫酸间发生了置换反应:Zn+H2SO4=ZnSO4+H2↑;
A、甲为铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,所以甲中铜片表面有气泡产生,故A错误;
B、乙不构成原电池,铜片不是电极,故B错误;
C、两装置中的反应均为Zn+H2SO4=ZnSO4+H2↑,所以两烧杯的溶液中氢离子浓度均减小,pH均增大,故C正确;
D、甲、乙装置中铜都不参加反应,所以甲、乙溶液都不变蓝,故D错误;
故选:C.
点评 本题考查了置换反应和原电池的有关知识,为高频考点,侧重元素化合物知识的综合理解以及原电池知识的理解和运用的考查,题目难度不大,注意把握原电池的组成条件的工作原理.

练习册系列答案
相关题目
11.恒容密闭容器中进行反应2SO2(g)+O2(g)?2SO3(g);△H<0以下说法正确的是( )
| A. | 若正反应速率V(SO2)=V(SO3).则反应达到平衡 | |
| B. | 若向容器中充入氦气.正、逆反应速率均增大 | |
| C. | 加入催化剂可以同时增加反应物和生成物的活化分子总数 | |
| D. | 到达化学平衡后加热会使正反应速率大于逆反应速率 |
8.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 60g丙醇存在的共价键总数为10 NA | |
| B. | 常温常压下,28 g C2H4和CO的混合气体中含有碳原子的数目为1.5NA | |
| C. | 7.2g新戊烷与异戊烷的混合物中所含极性共价键的数目为1.2NA | |
| D. | 标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA |
15.含有4个原子核,10个电子的微粒是( )
| A. | CH4 | B. | NH4+ | C. | H3O+ | D. | PH3 |
5.下列物质中不存在氢键的是( )
| A. | 乙醇 | B. | 乙酸 | C. | 苯酚 | D. | 苯 |
12.下列物质中能将苯酚水溶液、硫氰化钾溶液、乙酸、氢氧化钠溶液、硝酸银溶液一次区分开的是( )
| A. | 溴水 | B. | 石蕊溶液 | C. | 氯化铁溶液 | D. | 金属钠 |
9.下列化学用语正确的是( )
| A. | CH4分子的比例模型: | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 甲醛分子的电子式: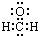 | D. | 基态硫原子的价电子排布:2s22p4 |
10.下列说法正确的是( )
| A. | HF比HCl稳定是由于HF分子间存在氢键所引起的 | |
| B. | 水在结冰时密度变小是由于水分子间存在氢键所引起的 | |
| C. | CH4分子很稳定,是由于分子间氢键的存在而导致的 | |
| D. | 离子化合物肯定含有金属元素,故在微粒间不存在共价键 |
 (s)+O2(g)=CO2(g)△H1 C(s)+1/2O2(g)=CO(g)△H2
(s)+O2(g)=CO2(g)△H1 C(s)+1/2O2(g)=CO(g)△H2