题目内容
臭氧可用于净化空气、饮用水消毒、处理工业废物和作为漂白剂。
(1)臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g)= 3Ag2O(s); △H=-236kJ·mol-1,
已知:2Ag2O(s)= 4Ag(s)+O2(g); △H=" +62" kJ·mol-1,
则O3转化为O2的热化学方程式为________________________________________________。
(2)臭氧在水中易分解,臭氧的浓度减少一半所需的时间如下表所示。
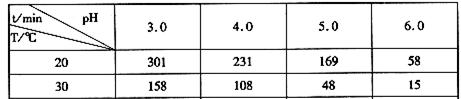
由上表可知pH增大能加速O3分解,表明对O3分解起催化作用的是__________(填微粒符号)。
(3)电解法臭氧发生器具有臭氧浓度高、成分纯净、在水中溶解度高的优势,在医疗、食品加工与养殖业及家庭方面具有广泛应用前景。科学家P.Tatapudi等人首先使用在酸性条件下电解水的方法制得臭氧。
臭氧在阳极周围的水中产生,其电极反应式为_______________________;阴极附近的氧气则生成过氧化氢,其电极反应式为_______________________。
(1)臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g)= 3Ag2O(s); △H=-236kJ·mol-1,
已知:2Ag2O(s)= 4Ag(s)+O2(g); △H=" +62" kJ·mol-1,
则O3转化为O2的热化学方程式为________________________________________________。
(2)臭氧在水中易分解,臭氧的浓度减少一半所需的时间如下表所示。

由上表可知pH增大能加速O3分解,表明对O3分解起催化作用的是__________(填微粒符号)。
(3)电解法臭氧发生器具有臭氧浓度高、成分纯净、在水中溶解度高的优势,在医疗、食品加工与养殖业及家庭方面具有广泛应用前景。科学家P.Tatapudi等人首先使用在酸性条件下电解水的方法制得臭氧。
臭氧在阳极周围的水中产生,其电极反应式为_______________________;阴极附近的氧气则生成过氧化氢,其电极反应式为_______________________。
(1)2O3=3O2 △H="-286kJ/mol" (3分)(2)OH- (1分)
(3)3H2O-6e-=O3↑+6H+ (3分) 3O2+6H++6e-=3H2O2(3分)
(3)3H2O-6e-=O3↑+6H+ (3分) 3O2+6H++6e-=3H2O2(3分)
试题分析:(1)①6Ag(s)+O3(g)=3Ag2O(s)△H=-235.8kJ?mol-1,②2Ag2O(s)=4Ag(s)+O2(g)△H=+62.2kJ?mol-1,根据盖斯定律可知①×2+②×3可得到,2O3(g)=3O2(g),则反应热△H=(-235.8kJ?mol-1)×2+(+62.2kJ?mol-1)×3=-285kJ/mol,所以热化学方程式为2O3(g)=3O2(g)△H=-285kJ/mol(2)由表格中的数据可知,相同温度下,pH越大,O3分解速率越大,表明对O3分解起催化作用的是OH-(3) 酸性条件下电解水的方法制得臭氧.臭氧在阳极周围的水中产生,其电极反应式为3H2O-6e-=O3↑+6H+,阴极附近的氧气则生成过氧化氢,其电极反应式为3O2+6H++6e-=3H2O2

练习册系列答案
相关题目
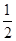 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2 O2(g) ===CO(g);ΔH1 C(s)+O2(g) ===CO2(g);ΔH2
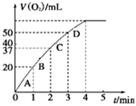
O2(g) ===CO(g);ΔH1 C(s)+O2(g) ===CO2(g);ΔH2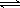 2NH3 △H ="-92.4" kJ/mol,开始他们将N2和H2混合气体20mol (体积比1:1)充入5L合成塔中.反应前压强为P0,反应过程中压强用P表示,反应过程中P/P0与时间t的关系如图所示。请回答下列问题:
2NH3 △H ="-92.4" kJ/mol,开始他们将N2和H2混合气体20mol (体积比1:1)充入5L合成塔中.反应前压强为P0,反应过程中压强用P表示,反应过程中P/P0与时间t的关系如图所示。请回答下列问题: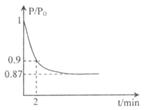
 CH3OH(g) △H
CH3OH(g) △H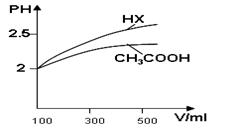
 2NO(g) ΔH,已知该反应在 T ℃时,平衡常数K=9.0。
2NO(g) ΔH,已知该反应在 T ℃时,平衡常数K=9.0。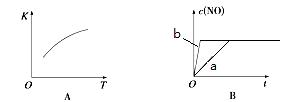
 CH3OH(g) ΔH1
CH3OH(g) ΔH1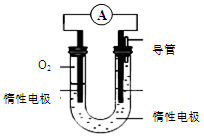
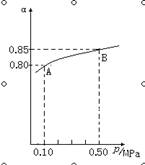
 2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题: