题目内容
二氧化氯(ClO2)是一种新型的自来水消毒剂,下列关于它的描述错误的是( )
分析:A.氧化物由两种元素组成,其中一种为氧元素;
B.在二氧化氯(C102)中,氧元素的化合价为-2价,可根据化合物中各元素正负化合价的代数和为零计算氯元素的化合价;
C.由二氧化氯(C102)知,它是由分子构成的物质;
D.根据各种元素的相对原子质量的总和.
B.在二氧化氯(C102)中,氧元素的化合价为-2价,可根据化合物中各元素正负化合价的代数和为零计算氯元素的化合价;
C.由二氧化氯(C102)知,它是由分子构成的物质;
D.根据各种元素的相对原子质量的总和.
解答:解:A.由二氧化氯(C102)可知该物质是由氯元素和氧元素组成的氧化物,故A正确;
B.在二氧化氯(C102)中,氧元素的化合价为-2价,可根据化合物中各元素正负化合价的代数和为零计算氯元素的化合价为+4价,故B正确;
C.由二氧化氯(C102)知,分子是由氯原子和氧原子直接构成,不存在氧气分子,故C错误;
D.由二氧化氯(C102)知其相对分子质量=35.5+16×2=67.5,故D正确.
故选C.
B.在二氧化氯(C102)中,氧元素的化合价为-2价,可根据化合物中各元素正负化合价的代数和为零计算氯元素的化合价为+4价,故B正确;
C.由二氧化氯(C102)知,分子是由氯原子和氧原子直接构成,不存在氧气分子,故C错误;
D.由二氧化氯(C102)知其相对分子质量=35.5+16×2=67.5,故D正确.
故选C.
点评:本题考查含氯化合物知识,要求学生了解化学式的书写及其意义,从组成上识别氧化物,并了解有关化学式的计算和推断方法及其技巧,难度不大.

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.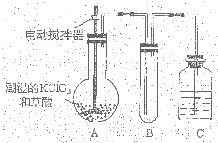 二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用下图所示装置模拟工业制取及收集ClO2.(夹持仪器已省略).回答问题:
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水.ClO2可以看做是亚氯酸(HClO2)和氯酸(HClO3)的混合酸酐.工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用下图所示装置模拟工业制取及收集ClO2.(夹持仪器已省略).回答问题: