题目内容
10.氯气是一种重要的化工原料,在生产、生活中有着重要的应用.请你根据所学知识回答下列问题:I.把氯气通入紫色石蕊试液中,可以观察到的现象是溶液先变红后退色;氯气常用于自来水消毒,请写出氯气与水反应的化学方程式:Cl2+H2O=HCl+HClO.
II.某化学兴趣小组计划用氯气和氢氧化钠溶液制取简易消毒液.其反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O;
III.工业上用氯气和石灰乳反应制漂白粉.漂白粉长时期露至在空气中会失效,用化学方程式表示其失效的原因:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;2HClO $\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
分析 Ⅰ.氯气溶于水,部分与水反应生成盐酸和次氯酸,盐酸具有酸性,次氯酸具有漂白性;
II.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水;
III.次氯酸酸性弱于碳酸,次氯酸钙与空气中二氧化碳和水反应生成次氯酸和碳酸钙,次氯酸不稳定见光分解生成氯化氢和氧气.
解答 解:Ⅰ.氯气溶于水,部分与水反应生成盐酸和次氯酸,盐酸具有酸性,次氯酸具有漂白性,化学方程式:Cl2+H2O=HCl+HClO,所以看到溶液先变红后退色;
故答案为:溶液先变红后退色; Cl2+H2O=HCl+HClO;
II.氯气与氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,化学方程式:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
III.漂白粉长时期露至在空气中,次氯酸钙与空气中二氧化碳和水反应生成次氯酸和碳酸钙,化学方程式:
Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;次氯酸不稳定见光分解生成氯化氢和氧气,方程式:2HClO $\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑;
故答案为:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO; 2HClO $\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑.
点评 本题考查了氯气的性质,熟悉氯气与水的反应,明确氯水中所含微粒及微粒性质是解题关键,注意漂白粉的主要成分与有效成分的区别,题目难度不大.

练习册系列答案
 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
20.下列贮存化学试剂的方法正确的是( )
| A. | 新制的氯水保存在棕色广口瓶中,并放在阴凉处 | |
| B. | 用做感光片的溴化银贮存在无色试剂瓶中 | |
| C. | 烧碱溶液放在带磨口玻璃塞的试剂瓶中 | |
| D. | 1mol/L NaCl溶液不能长期保存在容量瓶中 |
1.下列说法错误的是( )
| A. | Fe与S混合加热生成FeS | |
| B. | Al箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al 并不滴落 | |
| C. | 检验SO2气体中是否含有CO2气体,可将气体先通入饱和碳酸氢钠溶液,再通入品红溶液,最后通入澄清石灰水溶液 | |
| D. | 氯化氢水溶液能导电,所以氯化氢是电解质 |
15.镍镉电池是一种可充电电池,该电池放电时的总反应为:Cd+2NiOOH+2H2O=Cd(OH)2+2Ni(OH)2 下列说法错误的是( )
| A. | 该电池的电解液可以选用KOH溶液,负极是Cd,正极是NiOOH | |
| B. | 该电池放电时,负极反应为:Cd-2e-+2OH-=Cd(OH)2 | |
| C. | 该电池充电过程中,阴极附近的溶液PH降低 | |
| D. | 该电池充电时,阳极反应为:2Ni(OH)2-2e-+2OH-=2NiOOH+2H2O |
2.已知氟化氢气体中有平衡关系:
2H3F3(g)?3H2F2(g)△H1=a kJ•mol-1
H2F2 (g)?2HF (g)△H2=b kJ•mol-1
已知a、b均大于0;则可推测反应:H3F3(g)?3HF(g)的△H3为( )
2H3F3(g)?3H2F2(g)△H1=a kJ•mol-1
H2F2 (g)?2HF (g)△H2=b kJ•mol-1
已知a、b均大于0;则可推测反应:H3F3(g)?3HF(g)的△H3为( )
| A. | +(a+b)kJ•mol-1 | B. | +(a-b)kJ•mol-1 | ||
| C. | +(a+3b)kJ•mol-1 | D. | +(0.5a+1.5b)kJ•mol-1 |
19.欲使CuSO4•5H2O和SiO2的混合物分离开来,其必要的实验操作为( )
| A. | 加热 溶解 过滤 结晶 | B. | 溶解 过滤 蒸发 结晶 | ||
| C. | 加热 溶解 蒸发 过滤 | D. | 溶解 过滤 蒸馏 蒸发 |
20. 向某分散系中逐滴加入硫酸,测得溶液中沉淀的质量与加入硫酸的物质的量的关系如图所示,则该分散系可能是( )
向某分散系中逐滴加入硫酸,测得溶液中沉淀的质量与加入硫酸的物质的量的关系如图所示,则该分散系可能是( )
 向某分散系中逐滴加入硫酸,测得溶液中沉淀的质量与加入硫酸的物质的量的关系如图所示,则该分散系可能是( )
向某分散系中逐滴加入硫酸,测得溶液中沉淀的质量与加入硫酸的物质的量的关系如图所示,则该分散系可能是( )| A. | 硝酸钙与硫酸钾的混合液 | B. | 氯化钡与碳酸钠的混合液 | ||
| C. | 硫酸镁与氢氧化钾的混合液 | D. | 氯化铝与硝酸钠的混合液 |


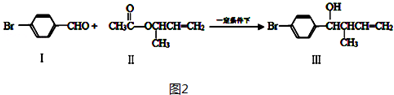
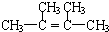
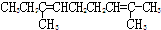 .
.