题目内容
2mol O3和3mol O2的质量(填“相等”、“不相等”或“无法判断”)
相等
相等
分子数之比为2:3
2:3
;所含氧原子的数目之比为1:1
1:1
;标准状况下,体的体积之比为2:3
2:3
.分析:根据m=nM计算O2和O3的质量,进而比较二者质量的大小;根据数目之比等于物质的量之比;根据O3和O2的物质的量以及分子的组成来计算原子的物质的量,原子数目之比等于物质的量之比;同温同压下体积之比等于物质的量之比.
解答:解:2molO3的质量为2mol×48g/mol=96g,3molO2的质量为3mol×32g/mol=96g,故二者质量相等;
2molO3和3molO2的数目之比等于物质的量之比,即分子数之比为2mol:3mol=2:3;
2molO3中O原子的物质的量为2mol×3=6mol,3mol O2的中O原子的物质的量为3mol×2=6mol,所含氧原子的数目之比为6mol:6mol=1:1;
同温同压下体积之比等于物质的量之比,故2molO2和与3molO3的体积之比为2mol:3mol=2:3,
故答案为:相等;2:3;1:1;2:3;
2molO3和3molO2的数目之比等于物质的量之比,即分子数之比为2mol:3mol=2:3;
2molO3中O原子的物质的量为2mol×3=6mol,3mol O2的中O原子的物质的量为3mol×2=6mol,所含氧原子的数目之比为6mol:6mol=1:1;
同温同压下体积之比等于物质的量之比,故2molO2和与3molO3的体积之比为2mol:3mol=2:3,
故答案为:相等;2:3;1:1;2:3;
点评:本题主要考查常用化学计量的有关计算、物质中原子数目的计算等,比较基础,注意根据化学式确定原子数目与物质的物质的量关系.

练习册系列答案
相关题目
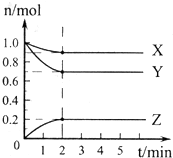 (1)某温度下,在一密闭容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如下图所示.分析有关数据,写出X、Y、Z反应的化学方程式
(1)某温度下,在一密闭容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如下图所示.分析有关数据,写出X、Y、Z反应的化学方程式