题目内容
请判断下列原电池的正负极:
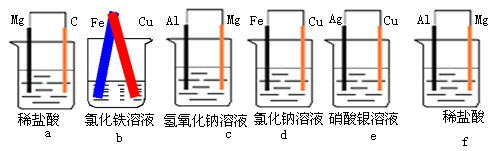
___________________________________________________
a中,负极Mg,正极C,电池反应式为Mg +2H+=Mg2+ +H2↑
b中,负极Fe,正极Cu,电池反应式为Fe+ 2Fe3+ =3Fe2+
c中,负极Al,正极Mg,电池反应式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑
d中,负极Fe,正极Cu,电池反应式为2Fe+2H2O+O2=2Fe(OH)2
e中,负极Cu,正极Ag,电池反应式为Cu +2Ag+=Cu2+ + 2Ag
f中,负极Mg,正极Al,电池反应式为Mg+2H+=Mg2+ +H2↑
b中,负极Fe,正极Cu,电池反应式为Fe+ 2Fe3+ =3Fe2+
c中,负极Al,正极Mg,电池反应式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑
d中,负极Fe,正极Cu,电池反应式为2Fe+2H2O+O2=2Fe(OH)2
e中,负极Cu,正极Ag,电池反应式为Cu +2Ag+=Cu2+ + 2Ag
f中,负极Mg,正极Al,电池反应式为Mg+2H+=Mg2+ +H2↑

练习册系列答案
相关题目
(12分)某化学兴趣小组利用下图所示原电池装置进行实验,请回答下列问题:
(1)实验中,同学们发现两装置电流计的指针偏转方向不同,因此有人提出以下观点,其中正确的是____________。(双选题,漏选得1分,多选错选得0分)
| A.金属活动性铝比镁强 |
| B.金属活动性镁比铝强,两装置中镁均为负极 |
| C.仅根据金属活动性顺序不能准确判断原电池的正负极 |
| D.原电池中的正负极受电解质溶液的酸碱性、强氧化性等因素的影响 |
①正极:__________________________________________;
②负极:__________________________________________。
(3)乙图中铝片与NaOH溶液反应的总化学方程式为______________________。某同学测得乙图中实验前铝片的质量是10g,实验后的质量是4.6g,则在实验过程中产生氢气的体积为 L(标况),转移电子的物质的量为 mol。


