题目内容
(6分)

(1)①用1.0 mol·L-1盐酸配制100 mL 0.10 mol·L-1盐酸,所需的玻璃仪器有量筒、
100 mL容量瓶、烧杯、 、 。
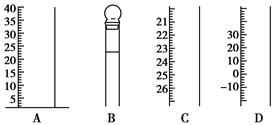
②用0.10 mol·L-1标准盐酸滴定未知浓度的烧碱溶液时,酸式滴定管初读教为0.10
mL,终读数如右图所示,则滴定所用盐酸体积为____。
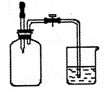
(2)如右图所示,集气瓶内充满某混合气体,置于光亮处一段时间,
将滴管内的水挤入集气瓶,再打开止水夹,烧杯中的水会进入
集气瓶。该集气瓶中的气体可能是 。

(1)①用1.0 mol·L-1盐酸配制100 mL 0.10 mol·L-1盐酸,所需的玻璃仪器有量筒、
100 mL容量瓶、烧杯、 、 。
②用0.10 mol·L-1标准盐酸滴定未知浓度的烧碱溶液时,酸式滴定管初读教为0.10
mL,终读数如右图所示,则滴定所用盐酸体积为____。
(2)如右图所示,集气瓶内充满某混合气体,置于光亮处一段时间,
将滴管内的水挤入集气瓶,再打开止水夹,烧杯中的水会进入
集气瓶。该集气瓶中的气体可能是 。

| A.CO、O2 |
| B.Cl2、CH4 |
| C.NO2、O2 |
| D.N2、H2 |

略

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目