题目内容
反应NO+O2+NO2+H2O→HNO3(未配平),是多组化学计量数的化学方程式,当氧气有1/3被NO还原时,该反应各物质化学计量数之比为
- A.4∶9∶24∶14∶28
- B.1∶1∶1∶1∶2
- C.8∶9∶12∶10∶20
- D.任意比均可
A
导解:设氧气为3mol,
4NO~ 3O2, 4NO2~O24/3mol 1mol 8mol 2mol 所以n(NO)∶n(O2)∶n(NO2)=4/3∶3∶8=4∶9∶24.
导解:设氧气为3mol,
4NO~ 3O2, 4NO2~O24/3mol 1mol 8mol 2mol 所以n(NO)∶n(O2)∶n(NO2)=4/3∶3∶8=4∶9∶24.

练习册系列答案
相关题目
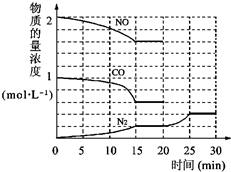 中NO(g)、CO(g)、N2(g)的物质的量浓度变化如图所示,则反应进行到15min时,NO的平均反应速率为
中NO(g)、CO(g)、N2(g)的物质的量浓度变化如图所示,则反应进行到15min时,NO的平均反应速率为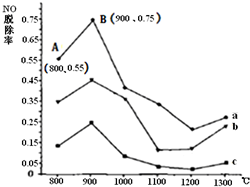 (2013?朝阳区一模)燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放.
(2013?朝阳区一模)燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放. (2010?泰州二模)下图为工业制备硝酸的设备示意图,其生产过程中发生的反应主要有:
(2010?泰州二模)下图为工业制备硝酸的设备示意图,其生产过程中发生的反应主要有: 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块铜片,再用滴管滴入10mL稀硝酸.据此回答下列问题:
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块铜片,再用滴管滴入10mL稀硝酸.据此回答下列问题: