题目内容
【题目】下列晶体中,化学键种类相同、晶体类型也相同的是( )
A. SO3与SiO2 B. NO2与H2O C. NaCl与HCl D. CCl4与KCl
【答案】B
【解析】A. SO3含有共价键,属于分子晶体,SiO2含有共价键,属于原子晶体,晶体类型不同;B. NO2含有共价键,属于分子晶体,H2O含有共价键,属于分子晶体,化学键种类相同、晶体类型也相同;C. NaCl含有离子键,属于离子晶体,HCl含有共价键,属于分子晶体,化学键种类不同、晶体类型也不同;D. CCl4含有共价键,属于分子晶体,KCl含有离子键,属于离子晶体,化学键种类不同、晶体类型也不同。故选B。

【题目】已知A、B、C、D、E、F均为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的P亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子,B离子与E离子具有相同的电子层结构,可形成E2B2、E2B型化合物。F元素位于元素周期表的ds区,且d亚层电子全满,其原子与E原子具有相同的最外层电子数。
请回答下面的问题:
(1)根据以上信息推断:①B元素为____________(写元素名称)
②F原子核外的价电子排布为____________。
(2)指出在元素周期表中:①D元素在______区;②E元素在______区。
(3)当n =2时,A与氢元素形成的相对分子质量为26的分子应属于______分子(填“极性"或“非极性”),该分子中有______个σ键______个π键。
(4)当n=3时,A与B形成的晶体属于______晶体。A单质的晶体结构中,A原子采用______杂化,A原子数与A-A键数之比为____________。
(5)DCl2分子中,中心原子D有______对孤对电子,用价层电子对互斥模型推测:DCl2分子的空间构型为________形。
(6)A—F六种元素中,有一种元素的部分电离能数据如下,它可能是 ______(写元素符号)(其中I1 —I7分别表示该元素的第一电离能——第七电离能)。
电离能 | I1 | I2 | I3 | I4 | I5 | I6 | I7 |
(KJ.mol-1) | 14.5 | 29.6 | 47.4 | 77.5 | 97.9 | 551.9 | 666.8 |
(7)元素F的某种氧化物的晶体晶胞结构如下图所示,其中实心球表示F原子,则该氧化物的化学式为____________。

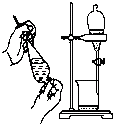
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( ) 
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A.A
B.B
C.C
D.D