��Ŀ����
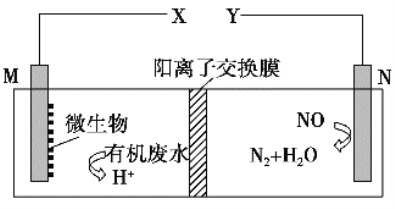
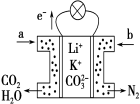
����Ŀ����ͭ��һ�㺬��п����������������ʡ�����ͼ��ʾ��װ���У��׳ص��ܷ�Ӧ����ʽΪ2CH3OH��3O2��4KOH��2K2CO3��6H2O����ͨ��·һ��ʱ���Cu�缫����������3.2g���ڴ˹����У�����˵����ȷ����
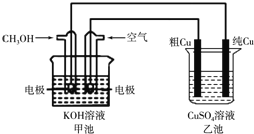
A. �ҳ���CuSO4��Һ��Ũ�Ȳ���
B. �׳������������ı�״���¿����������2.8L��������O2���������20%���㣩
C. �׳��ǵ���ת��Ϊ��ѧ�ܵ�װ�ã��ҳ��ǻ�ѧ��ת��Ϊ���ܵ�װ��
D. �׳�ͨ��CH3OHһ���ĵ缫��ӦΪ��CH3OH��6e����2H2O��CO32����8H��
���𰸡�B
��������������A���ҳ�Ϊ��ͭ�ĵ�⾫�������ݵ��ԭ��������
B������ת�Ƶ����غ�������Ŀ��������
C���׳���ԭ��ء��ҳ��ǵ��أ�
D��ͨ��״��ĵ缫�Ǹ����������ϼ״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ��
��⣺A���ҳ�Ϊ��ͭ�ĵ�⾫������ͭ�缫��Cu����������ʧ���ӡ���ͭ������������ֻ��Cu��������Һ��ͭ���Ӽ��٣�����Һ��ͭ����Ũ�Ƚ��ͣ�A����
B��3.2gͭ�����ʵ�����0.05mol��ת�Ƶ�����0.1mol��������·��ת�Ƶ�����ȣ�����3.2gͭת�Ƶ��ӵ����ʵ���=�����õ��ӵ����ʵ���������Ҫ������0.1mol��4��0.025mol���������Ŀ������Ϊ0.025mol��5��22.4L/mol��2.8L��B��ȷ��
C���׳���ԭ��ء��ҳ��ǵ��أ����Լ׳��ǽ���ѧ��ת��Ϊ���ܵ�װ�á��ҳ��ǽ�����ת��Ϊ��ѧ�ܵ�װ�ã�C����
D��ͨ��״��ĵ缫�Ǹ����������ϼ״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪCH3OH-6e-+8OH-��CO32-+6H2O��D����ѡB��

����Ŀ��X��Y��Z��M��R��Q�Ƕ���������Ԫ�أ�������Ϣ���±���ʾ��
X | Y | Z | M | R | Q | |
ԭ�Ӱ뾶 | 0.186 | 0.074 | 0.099 | 0.143 | ||
��Ҫ���ϼ� | ��4����4 | ��2 | ��1����7 | ��3 | ||
���� | ������������� | ���ǽ������ϵ����� | ��ɫ��Ӧ�ʻ�ɫ |
��1��X��M��ԭ�ӿɹ���18���ӵķ��ӣ��÷��ӵķ���ʽΪ______________��
��2��Z��Q��ȣ������Խ�ǿ����______________����Ԫ�ط��ű�ʾ����������ʵ��֤��һ���۵���______________������ĸ���ţ���
A.Q���۵��Z���۵�ߣ�Q��Ӳ�ȱ�Z��Ӳ�ȴ�
B.Z����ˮ��ӦѸ�٣���Q����ˮ��������Ӧ
C.Z������������Ӧˮ������ǿ���Q������������Ӧˮ�����������
��3����YԪ��ͬ����Ķ�����Ԫ��E����Ȼ���д��ڶ��ֺ��أ�����֮��Ĺ�ϵ��Ϊ_______________��
��4��д��Z2M2�ĵ���ʽ��___________________��