题目内容
【题目】化合物F是合成抗过敏药孟鲁司特钠的重要中间体,其合成过程如下:
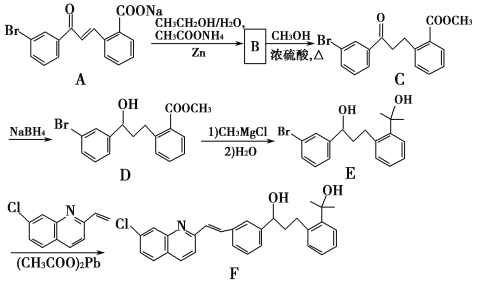
请回答下列问题:
(1)化合物B的分子式为C16H13O3Br,B的结构简式为_________。
(2)由C→D、E→F的反应类型依次为_________、_________。
(3)写出符合下列条件C的一种同分异构体的结构简式_________。
Ⅰ属于芳香族化合物,且分子中含有2个苯环
Ⅱ能够发生银镜反应
Ⅲ分子中有5种不同环境的氢原子。
(4)已知:RCl![]() RMgCl,写出以CH3CH2OH、
RMgCl,写出以CH3CH2OH、![]() 为原料制备
为原料制备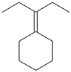 的合成路线流程图(乙醚溶剂及无机试剂任用)。合成路线流程图示例见本题题干。____________
的合成路线流程图(乙醚溶剂及无机试剂任用)。合成路线流程图示例见本题题干。____________
【答案】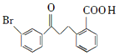 加成反应 取代反应
加成反应 取代反应 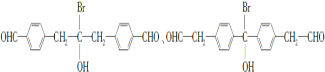
【解析】
B发生酯化反应生成C,根据C结构简式知,B结构简式为 ,C发生加成反应生成D,D反应生成E,E发生取代反应生成F。
,C发生加成反应生成D,D反应生成E,E发生取代反应生成F。
(1)B发生酯化反应生成C,根据C结构简式知,B结构简式为 ;
;
(2)根据合成过程可知,![]() :加成反应,
:加成反应,![]() :取代反应;
:取代反应;
(3)C的同分异构体符合下列条件:Ⅰ属于芳香族化合物,且分子中含有2个苯环;Ⅱ能够发生银镜反应说明含有醛基;Ⅲ分子中有5种不同环境的氢原子;可得到:
符合条件的同分异构体结构简式为 ;
;
(4)已知:![]() 可知,
可知,![]() 与
与![]() 发生取代反应生成
发生取代反应生成![]() ,
,![]() 与
与![]() 、乙醚反应生成
、乙醚反应生成![]() ,
,![]() 与
与
![]() 反应,然后水解生成
反应,然后水解生成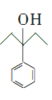 ,
, 和氢气发生加成反应生成
和氢气发生加成反应生成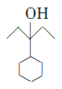 ,
, 在浓硫酸加热条件下发生消去反应,生成
在浓硫酸加热条件下发生消去反应,生成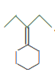 ,
,
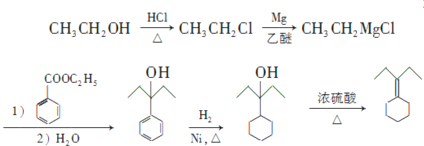
其合成线路流程为:

【题目】采用N2O5为硝化剂是一种新型的绿色硝化技术,F.Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
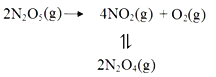
其中NO2二聚为N2O4的反应可以迅速达到平衡,体系的总压强p随时间t的变化如下表所示(t=∞时,N2O5(g)完全分解):
t/min | 0 | 40 | 80 | 160 | 260 | 1300 | 1700 | ∞ |
p/kPa | 35.8 | 40.3 | 42.5 | 45.9 | 49.2 | 61.2 | 62.3 | 63.1 |
(1)已知:2N2O5(g)=2N2O4(g)+O2(g) △H1=-4.4 kJ· mol-1
N2O4(g)![]() 2NO2(g) △H2=+55.3 kJ· mol-1
2NO2(g) △H2=+55.3 kJ· mol-1
则反应N2O5(g)=2NO2(g)+![]() O2(g)的 △H=________kJ· mol-1。
O2(g)的 △H=________kJ· mol-1。
(2)若提高反应温度至35℃,则N2O5(g)完全分解后体系压强介p∞(35℃)______63.1kPa(填“大于”“等于”或“小于”),原因是________________________________________________。
(3)25℃时N2O4(g)![]() 2NO2(g)反应的平衡常数Kp=________kPa (Kp为以分压表示的平衡常数,计算结保留1位小数)。下图中可以示意平衡常数Kp随温度T变化趋势的是_______。
2NO2(g)反应的平衡常数Kp=________kPa (Kp为以分压表示的平衡常数,计算结保留1位小数)。下图中可以示意平衡常数Kp随温度T变化趋势的是_______。

(4)邻二甲苯经硝化得到两种一硝化产物:3-硝基邻二甲苯(3-NOX)和4-硝基邻二甲苯(4-NOX)。某研究小组研究了采用N2O5为硝化剂时催化剂用量对该反应的影响。将一定量的催化剂和邻二甲苯置于反应瓶中,控制温度反应一定时间。测得邻二甲苯的转化率和3-NOX的选择性如图所示:
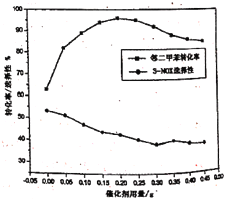
①描述并解释随着催化剂用量的增加,邻二甲苯转化率的变化趋势:____________。
②在图中画出4-NOX的选择性随催化剂用量变化的曲线_____________。