题目内容
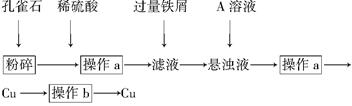
孔雀石的主要成分为Cu2(OH)2CO3。某校化学兴趣小组的同学设计从孔雀石中冶炼铜的方案如下:
回答下列问题:
(1)在粉碎后的孔雀石中加入稀硫酸,观察到的现象是_______________。
反应的离子方程式是___________________________________________。
(2)操作a中用到的玻璃仪器是____________________________________。
(3)A的化学式为________,在悬浊液中加入A的目的是______________。
(4)操作b包括洗涤和低温烘干,作用是__________________________。
(5)有同学认为,利用铁屑和稀硫酸,不通过上述实验方案,也能从孔雀石中冶炼铜。请你用简洁的文字说明不同方案的实验原理__________________。

回答下列问题:
(1)在粉碎后的孔雀石中加入稀硫酸,观察到的现象是_______________。
反应的离子方程式是___________________________________________。
(2)操作a中用到的玻璃仪器是____________________________________。
(3)A的化学式为________,在悬浊液中加入A的目的是______________。
(4)操作b包括洗涤和低温烘干,作用是__________________________。
(5)有同学认为,利用铁屑和稀硫酸,不通过上述实验方案,也能从孔雀石中冶炼铜。请你用简洁的文字说明不同方案的实验原理__________________。
(1)固体溶解,生成蓝色溶液和无色气体Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O
(2)玻璃棒、漏斗、烧杯
(3)H2SO4除去未反应的Fe
(4)除去杂质,得到纯净的铜
(5)先将孔雀石加热分解生成CuO,再用铁屑和稀硫酸反应产生的氢气在加热条件下还原CuO
(2)玻璃棒、漏斗、烧杯
(3)H2SO4除去未反应的Fe
(4)除去杂质,得到纯净的铜
(5)先将孔雀石加热分解生成CuO,再用铁屑和稀硫酸反应产生的氢气在加热条件下还原CuO
(1)孔雀石中有CO32-与稀硫酸反应会有CO2产生,Cu2+在溶液中显蓝色;Cu2(OH)2CO3+4H+=2Cu2++CO2↑+3H2O。(2)操作a应为过滤,过滤用的玻璃仪器为玻璃棒、漏斗、烧杯。(3)除去过量的铁粉应用稀H2SO4。(4)洗涤和低温烘干都是除去杂质。(5)孔雀石分解可生成CuO,H2SO4和Fe可生成H2,用氢气还原CuO生成铜。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
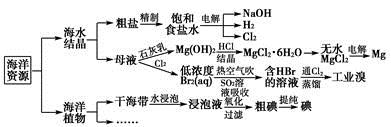
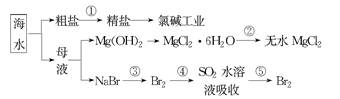
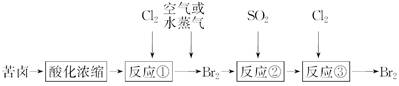
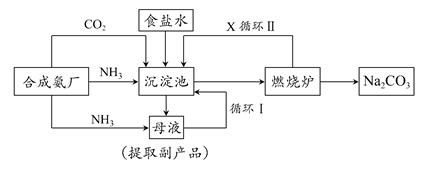
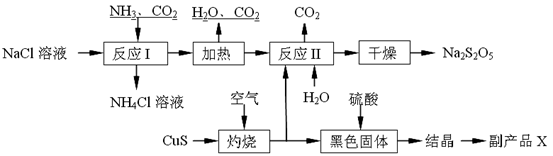
 Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。