题目内容
(8分)A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大。已知B的最外
电子层是ns2npn+1;C的p亚层上未成对的电子比B少一个,D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A能生成具有刺激性气味的气体。
(1)B核外电子排布式为__________________________。
(2)A与E化合时原子间以_____________键相结合,D与C化合时原子间以_____________键相结合。
(3)写出A、C直接形成的化合物与E的单质反应的离子方程式_______________________。
(4)写出B和D形成的化合物遇水时发生反应的方程式______________________________。
电子层是ns2npn+1;C的p亚层上未成对的电子比B少一个,D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A能生成具有刺激性气味的气体。
(1)B核外电子排布式为__________________________。
(2)A与E化合时原子间以_____________键相结合,D与C化合时原子间以_____________键相结合。
(3)写出A、C直接形成的化合物与E的单质反应的离子方程式_______________________。
(4)写出B和D形成的化合物遇水时发生反应的方程式______________________________。
(1)1s22s22p3 (2)共价;离子
(3)Cl2+H2O====H++Cl-+HClO
(4)Mg3N2+6H2O====3Mg(OH)2↓+2NH3↑
(3)Cl2+H2O====H++Cl-+HClO
(4)Mg3N2+6H2O====3Mg(OH)2↓+2NH3↑
由B的最外电子层是ns2npn+1结合其他条件可推知短周期中符合条件的为N:1s22s22p3,C的p亚层上未成对电子比B少一个,C为1s22s22p4应为O元素,D的二价阳离子与C的阴离子具有相同电子层结构,可知D为Mg,E与Mg同周期且在该周期中半径最小,应为Cl,能与N形成具有刺激性气味气体的A为H,由此可以解决以下几个具体问题。

练习册系列答案
相关题目
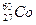 放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。
放射源进行了实验验证。次年,杨振宁、李政道两人因此获得诺贝尔物理奖。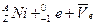

 B单质+A、C化合物
B单质+A、C化合物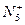 的盐类。Christe指出:
的盐类。Christe指出: 更强的氧化剂,跟水和有机物反应均发生爆炸。下列叙述错误的是( )
更强的氧化剂,跟水和有机物反应均发生爆炸。下列叙述错误的是( )