题目内容
【题目】S2Cl2是一种重要的化工产品。常温时是一种有毒并有恶臭的金黄色液体,熔点-76℃,沸点138℃,受热或遇水分解放热,放出腐蚀性烟气,易与水反应,300℃以上完全分解。进一步氯化可得 SCl2, SCl2 是樱桃红色液体,易挥发,熔点-122℃,沸点 59℃。SCl2与 S2Cl2 相似,有毒并有恶臭,但更不稳 定。实验室可利用硫与少量氯气在 110~140℃反应制得 S2Cl2 粗品。
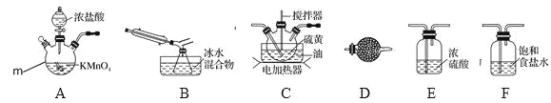
请回答下列问题:
(1)仪器 m 的名称为______,装置 D 中试剂的作用是______。
(2)装置连接顺序:______→B→D。
(3)为了提高 S2Cl2 的纯度,实验的关键是控制好温度和______。
(4)从 B 中分离得到纯净的 S2Cl2,需要进行的操作是______;
(5)若将S2Cl2放入少量水中会同时产生沉淀和两种气体。某同学设计了如下实验方案,测定所得混合气体中某一成分 X 的体积分数:
![]()
①W 溶液可以是______(填标号)。
a H2O2 溶液 b 氯水 c 酸性 KMnO4 溶液 d FeCl3 溶液
②该混合气体中气体 X 的体积分数为______(用含 V、m 的式子表示)。
【答案】三颈烧瓶 防止空气中的水蒸气进入B使产品与水反应,吸收剩余的Cl2 A→F→E→C 滴入浓盐酸的速率(或B中通入氯气的量) 蒸馏 a b ![]() ×100%
×100%
【解析】
本实验要硫与少量氯气在 110~140℃反应制备S2Cl2 粗品,根据题目信息“熔点-76℃,沸点138℃”,制备的产品为气体,需要冷凝收集;受热或遇水分解放热,所以温度要控制好,同时还要在无水环境进行制备,则氯气需要干燥除杂,且制备装置前后都需要干燥装置;所以装置连接顺序为A、F、E、C、B、D;
(5)S2Cl2遇水会生成SO2、HCl两种气体,实验目的是测定该混合气体中SO2的体积分数,混合气体通过溶液W溶液吸收二氧化硫气体得到溶液中加入加入过量氢氧化钡溶液反应得到硫酸钡沉淀,过滤洗涤干燥称量得到硫酸钡沉淀质量mg,据元素守恒计算二氧化硫体积分数。
(1)仪器m的名称为三颈烧瓶,装置D中试剂为碱石灰,作用为吸收Cl2,防止污染环境,防止外界水蒸气回流使S2Cl2分解;
(2)依据上述分析可知装置连接顺序为:A→F→E→C→B→D;
(3)反应生成S2Cl2的氯气过量则会生成SCl2,温度过高S2Cl2会分解,为了提高S2Cl2的纯度,实验的关键是控制好温度和滴入浓盐酸的速率或B中通入氯气的量;
(4)实验室制得S2Cl2粗品中含有SCl2杂质,根据题目信息可知二者熔沸点不同,SCl2易挥发,所以可通过蒸馏进行提纯;
(5)①W溶液的目的是氧化二氧化硫,可以是a:H2O2溶液,b:氯水,但不能是b:KMnO4溶液(硫酸酸化),因为高锰酸钾溶液能氧化氯化氢生成氯气,也不能用FeCl3 溶液会生成氢氧化铁成,故选:ab;
②过程分析可知生成沉淀为硫酸钡沉淀,硫元素守恒得到二氧化硫物质的量n(SO2)=n(BaSO4)=![]() =
=![]() mol,该混合气体中二氧化硫的体积分数为气体物质的量分数,二氧化硫体积分数=
mol,该混合气体中二氧化硫的体积分数为气体物质的量分数,二氧化硫体积分数= 。
。