题目内容
【题目】A是一种常见的单质,B、C为常见的化合物,A、B、C均含有元素x,它们有如图所示的转化关系(部分产物及反应条件已略去)。下列说法中正确的是( )
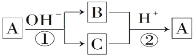
A. 反应①和②一定为氧化还原反应
B. 反应①和②互为可逆反应
C. X元素可能是金属,也可能是非金属
D. X元素可能为铝
【答案】A
【解析】
单质与强碱发生反应,生成了两种产物B和C,而且B和C均含有同一种元素,且B和C又可以在强酸的作用下发生反应,生成单质A,可以看出反应①是A物质的歧化反应,反应②应该是这种元素的归中反应,所以B和C中应该分别含有A的负价态物质以及正价态物质,故判断A一定是非金属元素。
A、①应该是A物质的歧化反应,反应②应该是一种元素的归中反应,则可以知道B和C中应该分别含有A的负价态物质以及正价态物质,所以反应①和②一定为氧化还原反应,故A正确;
B、可逆反应的定义是指在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应,上述①和②两个反应的反应条件不相同,不是可逆反应,故B错误;
C、A、B和C中都含有X元素,反应①是A物质的歧化反应,反应②应该是这种元素的归中反应,所以B和C中应该分别含有A的负价态物质以及正价态物质,判断A一定是非金属元素,因为金属元素无负价,说明X元素是非金属元素,故C错误;
D、A、B和C都含有X元素,反应①是A物质的歧化反应,反应②应该是这种元素的归中反应,所以B和C中应该分别含有A的负价态物质以及正价态物质,判断A一定是非金属元素,因为金属元素无负价,说明X元素是非金属元素,X元素肯定不能为铝,故D错误;
综上所述,本题应选A.

 名校课堂系列答案
名校课堂系列答案【题目】已知2A(g)+B(g)![]() 2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后,C的浓度为ω mol·L-1,放出的热量为b kJ。
2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后,C的浓度为ω mol·L-1,放出的热量为b kJ。
(1)已知:A(g)+X(g)![]() 2B(g) ΔH=-133.2 kJ·mol-1;
2B(g) ΔH=-133.2 kJ·mol-1;
5A(g)+X(g)![]() 4C(g) ΔH=-650.4 kJ·mol-1。则a=________。
4C(g) ΔH=-650.4 kJ·mol-1。则a=________。
(2)不同温度下该反应的平衡常数如表所示。由此可推知,表中T1________T2(填“>”“=”或“<”)。
T/K | T1 | T2 | T3 |
K | 1.00×107 | 2.45×105 | 1.88×103 |
若在原来的容器中,只加入2 mol C,500 ℃时充分反应达平衡后,吸收热量为c kJ,C的浓度________________ω mol·L-1(填“>”“=”或“<”),a、b、c之间的关系为________________。
(3)在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是________(填序号)。
A.4 mol A和2 mol B
B.4 mol A、2 mol B和2 mol C
C.4 mol A和4 mol B
D.6 mol A和4 mol B
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2 mol A和1 mol B,500 ℃时充分反应达平衡后,放出的热量为d kJ,则d________b(填“>”“=”或“<”),理由是____________________________________。
(5)在一定温度下,向一个容积可变的容器中,通入3 mol A和2 mol B及固体催化剂,充分反应,平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4 mol A、3 mol B和2 mol C,则平衡时A的百分含量________(填“不变”“变大”“变小”或“无法确定”)。