��Ŀ����
��2014�����ʡ�����и����ڶ���ģ�⿼�����ۻ�ѧ�Ծ���
��Ƴ���ͭ��ˮ�к���CN-��Cr2O72-����,��Ҫ������������ŷš��ó��ⶨ�������̽��з�ˮ������ �ش��������⣺
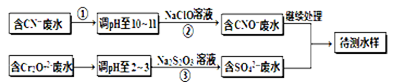
��1������������ˮ��������Ҫʹ�õķ����� ��
��2�����з�Ӧ��������ų����÷�Ӧ�����ӷ���ʽΪ ��
��3��������У�ÿ����0.4mol Cr2O72-ʱת�Ƶ���2.4mol���÷�Ӧ���ӷ���ʽΪ ��
��4��ȡ��������ˮ�����Թ��У�����NaOH��Һ���۲쵽����ɫ�������ɣ��ټ�Na2S��Һ�� ��ɫ����ת���ɺ�ɫ��������ʹ�û�ѧ��������ֽ��Ͳ����������ԭ�� ��
��5��Ŀǰ��������Cr2O72-��ˮ������������巨���÷������ˮ�м���FeSO4��7H2O��Cr2O72-��ԭ��Cr3+������pH��Fe��Crת�����൱��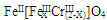 (��������,�������ֱ�ʾԪ�ؼ�̬)�ij���������1mol Cr2O72-�������a mol FeSO4?7H2O�����н�����ȷ���� ��
(��������,�������ֱ�ʾԪ�ؼ�̬)�ij���������1mol Cr2O72-�������a mol FeSO4?7H2O�����н�����ȷ���� ��
��Ƴ���ͭ��ˮ�к���CN-��Cr2O72-����,��Ҫ������������ŷš��ó��ⶨ�������̽��з�ˮ������ �ش��������⣺

��1������������ˮ��������Ҫʹ�õķ����� ��
��2�����з�Ӧ��������ų����÷�Ӧ�����ӷ���ʽΪ ��
��3��������У�ÿ����0.4mol Cr2O72-ʱת�Ƶ���2.4mol���÷�Ӧ���ӷ���ʽΪ ��
��4��ȡ��������ˮ�����Թ��У�����NaOH��Һ���۲쵽����ɫ�������ɣ��ټ�Na2S��Һ�� ��ɫ����ת���ɺ�ɫ��������ʹ�û�ѧ��������ֽ��Ͳ����������ԭ�� ��
��5��Ŀǰ��������Cr2O72-��ˮ������������巨���÷������ˮ�м���FeSO4��7H2O��Cr2O72-��ԭ��Cr3+������pH��Fe��Crת�����൱��
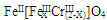 (��������,�������ֱ�ʾԪ�ؼ�̬)�ij���������1mol Cr2O72-�������a mol FeSO4?7H2O�����н�����ȷ���� ��
(��������,�������ֱ�ʾԪ�ؼ�̬)�ij���������1mol Cr2O72-�������a mol FeSO4?7H2O�����н�����ȷ���� ��| A��x ="0.5" ,a =8 | B��x ="0.5" ,a = 10 | C��x =" 1.5" ,a =8 | D��x =" 1.5" ,a = 10 |
(15��)��1��������ԭ��(3��) ��2��CN-+ClO-=CNO-+Cl-(3��)
��3��3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O(3��)
��4��Cu2++2OH-=Cu(OH)2�� Cu(OH)2(s)+S2-(aq)=CuS(s)+2OH-(aq)
����KSP(CuS)<KSP[Cu(OH)2] (3��) ��5��D(3��)
��3��3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O(3��)
��4��Cu2++2OH-=Cu(OH)2�� Cu(OH)2(s)+S2-(aq)=CuS(s)+2OH-(aq)
����KSP(CuS)<KSP[Cu(OH)2] (3��) ��5��D(3��)
��1��������ˮ������CN-��CNO-��Cr2O72-��Cr3+�����ʹ�õķ�����������ԭ����
��2�����з�ӦNaClO��CN-������������ų�������ΪCNO-������CN-+ClO-===CNO-+Cl-��
��3��������У���Ӧ��1mol Cr2O72-ʱת�Ƶ���6mol����Cr2O72-��Cr3+��3S2O32-+4Cr2O72-+26H+="==" 6SO42-+8Cr3++13H2O��
��4��ȡ��������ˮ�����Թ��У�����NaOH��Һ��������ɫ����Cu(OH)2���ټ�Na2S��Һ��Cu(OH)2ת���ɺ�ɫ����CuS(s)��˵��KSP(CuS)<KSP[Cu(OH)2]��
��5��������������y mol����Ѱ�ҹ�ϵ��
CrԪ�������䣬���У���2-x��y=2
FeԪ�������䣬���У���1+x)y=a
Feʧȥ�ĵ�����=Cr�õ��ĵ����������У�xy=2����6-3��=6
�ã�X=1.5��y=4��a=10

��ϰ��ϵ�д�
 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д�
�����Ŀ
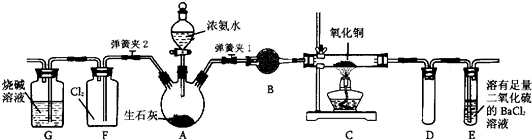

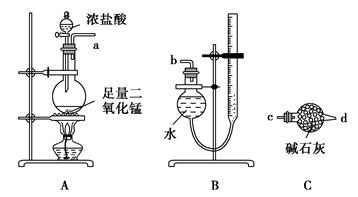
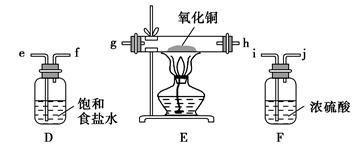
 2CuCl2��O2�ⶨͭ�Ľ������ԭ���������ɹ�ѡ���װ����ͼ��ʾ��
2CuCl2��O2�ⶨͭ�Ľ������ԭ���������ɹ�ѡ���װ����ͼ��ʾ��