题目内容
7.四种短周期元素在周期表中的位置如图,其中只有M为金属元素.下列说法不正确的是( )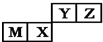
| A. | 原子半径:M>X>Y>Z | |
| B. | M的氯化物是弱电解质 | |
| C. | X的最简单气态氢化物的热稳定性比Z的小 | |
| D. | X的最高价氧化物不溶于任何酸 |
分析 根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,可知M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,以此解答该题.
解答 解:根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,可知M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,
A.一般来说原子核外电子层数越多,原子半径越大,同周期元素从左到右原子半径逐渐减小,则原子半径M>X>Y>Z,故A正确;
B.M为Al元素,对应的氯化物在溶液中完全电离,为强电解质,故B错误;
C.非金属性O>Si,水的稳定性较强,故C正确;
D.X为Si元素,对应的氧化物二氧化硅可溶于氢氟酸,故D错误.
故选BD.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,推断元素是解题关键,注意对元素周期表的整体把握,注意对元素周期律的理解掌握.

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目
18.下列实验目的能实现的是(部分夹持装置已略去)( )
| A. | 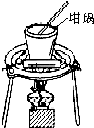 对溶液进行蒸发、浓缩、结晶 | |
| B. |  以己烯为萃取剂萃取溴水中的溴单质 | |
| C. | 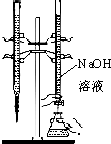 用已知浓度的氢氧化钠溶液滴定未知浓度的盐酸 | |
| D. | 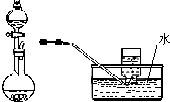 用稀硝酸与铜反应制取并收集NO |
2.下列体系中,离子能大量共存的是( )
| A. | 无色透明的酸性溶液:MnO4-、K+、C1-、SO42- | |
| B. | 使酚酞变红的溶液:K+、Na+、NO3-、Cl- | |
| C. | 滴加KSCN显红色的溶液:NH4+、K+、Cl-、I- | |
| D. | 0.1 mol•L-1NaHCO3溶液:Na+、Ba2+、NO3-、OH- |
19.下列叙述能证明金属A的金属性比金属B强的是( )
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子的电子层数少 | |
| C. | 1mol A从稀硫酸中置换的氢气比1mol B置换的氢气多 | |
| D. | 常温下,A能从冷水中置换出氢气,而B不能 |

 .
. 、、
、、 或
或 .
.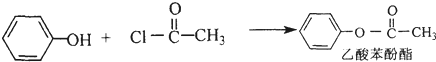 +HCl
+HCl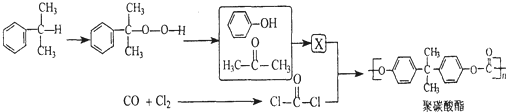
 .
. .
. .
. 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.