题目内容
【题目】在3Cl2+8NH3=6NH4Cl+N2反应中,以下说法不正确的是
A. 还原剂是NH3 ,
B. 该反应中每生成1mol N2则转移的电子数为6NA
C. 氧化性大小顺序为:Cl2> N2
D. Cl2和NH3都可以用碱石灰来干燥
【答案】D
【解析】在该反应中,氯气是氧化剂,氨气是还原剂,氯化铵为还原产物,氮气是氧化产物。氧化剂的氧化性大于氧化产物的氧化性。该反应中氮元素的化合价从-3升高到0,所以每生成1mol N2转移的电子数为6NA。D选项中,氯气是可以与碱反应的,所以氯气不能用碱性干燥剂干燥,氨气不与碱反应,所以氨气可以用碱石灰干燥。综上所述D不正确,选D。

【题目】1 L某混合溶液,可能含有的离子如表所示:
可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH |
可能大量含有的阴离子 | Cl-、Br-、I-、CO |
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。
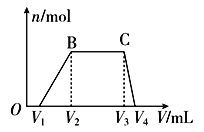
则该溶液中一定不含有的离子是________________________。
(2)BC段离子方程式为_______________________。
(3)V1、V2、V3、V4之间的关系为____________________。
(4)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 2.8 L | 5.6 L | 11.2 L |
n(Cl-) | 1.25 mol | 1.5 mol | 2 mol |
n(Br-) | 1.5 mol | 1.4 mol | 0.9 mol |
n(I-) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为________。
【题目】温度为T时.向2.0 L恒容密闭容器中充入1.0 mol PCl5,发生反应PCl5 (g)![]() PCl3(g)+Cl2(g),经过一段时间后达到平衡,反应过程中测定的部分数据列于下表。下列说法正确的是
PCl3(g)+Cl2(g),经过一段时间后达到平衡,反应过程中测定的部分数据列于下表。下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 在前50s,PCl3的平均反应速率 v(PCl3)=0.0032mol/(L·s)
B. 达到平衡时,容器中的压强是起始时的1.2倍
C. 相同温度下,起始时向容器中充入1.0mo PCl5、0.20 mo1 PCl3和0.20 mo1 Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%