题目内容
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)![]() 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示,下列说法错误的是()
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示,下列说法错误的是()
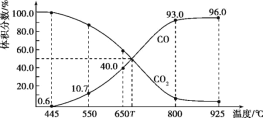
A.550 ℃时,若充入惰性气体,v正、v逆均减小,平衡向正反应方向移动
B.650 ℃时,反应达平衡后CO2的转化率为25.0%
C.T ℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= 23. 04p总
【答案】C
【解析】
A.550℃,若充入惰性气体,容器的压强不变,容器的体积增大,相当于减小压强,υ正、υ逆均减小,平衡向正反应方向移动,A正确;
B.由图知650℃时,CO的体积分数为40%,CO2的体积分数为60%,平衡时n(CO2):n(CO)=60%:40%=3:2,设CO2平衡物质的量为3mol,CO平衡物质的量为2mol,生成2molCO消耗1molCO2,反应达到平衡时CO2的转化率为![]() 100%=25%,B正确;
100%=25%,B正确;
C.T℃平衡时CO与CO2的体积分数相等,若充入等体积的CO2和CO即为平衡状态,平衡不移动,C错误;
D.925℃时CO的体积分数为96%,CO2的体积分数为4%,CO的分压为0.96p总,CO2的分压为0.04p总,用平衡分压代替平衡浓度表示的化学平衡常数Kp=![]() =23.04p总;D正确;
=23.04p总;D正确;
故选C。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】工业上以菱镁矿(主要成分为MgCO3含少量FeCO3)为原料制备金属镁的实验流程如下:
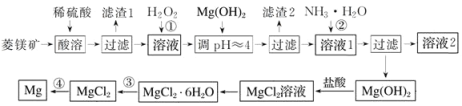
已知:一些金属离转化为氢氧化物沉淀时溶液的pH如表所示
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
完全沉淀时 | 3.7 | 5.2 | 9.7 |
请回答:
(1)上述流程中H2O2的作用是:_____________
(2)滤渣2的主要成分为:_______________;溶液2中的主要溶质为:__________________。
(3)通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,为保证Mg2+沉淀完全,过程②中控制溶液的pH至少为__________________(保留小数点后一位)(已知Mg(OH)2的Ksp=2×10-11,lg2=0.3)
(4)已知MgCl2·6H2O受热时发生水解:MgCl2·6H2O=Mg(OH)Cl+HCl↑+H2O,过程③应该如何操作才能得到无水MgCl2__________________
(5)写出过程④中发生反应的化学方程式:____________________________________