��Ŀ����
T1��ʱ�����ݻ�Ϊ2L���ܱ������г���һ������A�����B���壬�������·�Ӧ��
A(g)��2B (g) C(g)
C(g)
��Ӧ�����вⶨ�IJ������ݼ��±���
����˵����ȷ����
A��ǰ10 min�ڷ�Ӧ��ƽ������Ϊv(C)��0.050 mol��L��1��min��1
B�����������������䣬��ʼʱ�������г���0.50 mol A�����0.60 mol B���壬����ƽ��ʱ��n(C)��0.25 mol
C�����ܱ���������ɱ䣬�����������䣬�ڴﵽƽ��������С�����������ƽ��һֱ�������ƶ�
D���¶�ΪT2��ʱ��T1��T2����������Ӧƽ�ⳣ��Ϊ20��������ӦΪ���ȷ�Ӧ
A(g)��2B (g)
 C(g)
C(g)��Ӧ�����вⶨ�IJ������ݼ��±���
| ��Ӧʱ��/min | n(A)/mol | n(B)/ mol |
| 0 | 1.00 | 1.20 |
| 10 | 0.50 | |
| 30 | | 0.20 |
����˵����ȷ����
A��ǰ10 min�ڷ�Ӧ��ƽ������Ϊv(C)��0.050 mol��L��1��min��1
B�����������������䣬��ʼʱ�������г���0.50 mol A�����0.60 mol B���壬����ƽ��ʱ��n(C)��0.25 mol
C�����ܱ���������ɱ䣬�����������䣬�ڴﵽƽ��������С�����������ƽ��һֱ�������ƶ�
D���¶�ΪT2��ʱ��T1��T2����������Ӧƽ�ⳣ��Ϊ20��������ӦΪ���ȷ�Ӧ
BC
���������A��ǰ10 min�ڷ�Ӧ��ƽ������Ϊv(C)��2v(A)��0.5/2/10="0.025" mol��L��1��min��1�������ݱ��е����ݣ������Ʋ���30����ʱ�ﵽƽ�⣬��ʱƽ�ⳣK=0.1/(0.4)*(0.4)2=25/1.6<20��˵���¶�ΪT2��ʱ�������¿�ƽ�������ƶ������淴ӦΪ���ȷ�Ӧ����������ӦӦ�������ȷ�Ӧ

��ϰ��ϵ�д�
 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
�����Ŀ
 CH3OH(g)��H2O(g) ��H =��49.0 kJ��mol��1
CH3OH(g)��H2O(g) ��H =��49.0 kJ��mol��1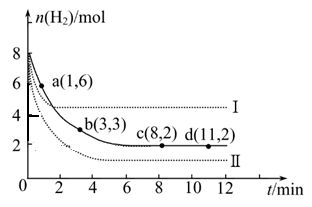

 2H2O
2H2O 2NH3(g) ��H����92.20 kJ��mol��1��
2NH3(g) ��H����92.20 kJ��mol��1�� C(g)+2D(g) ��H<0��ƽ��ʱC�����ʵ��������B�����ʵ����ı仯��ϵ��ͼ��ʾ������˵����ȷ����( )
C(g)+2D(g) ��H<0��ƽ��ʱC�����ʵ��������B�����ʵ����ı仯��ϵ��ͼ��ʾ������˵����ȷ����( )
 2NH3(g)+92.4 kJ/mol673K��30MPa�£������ϳɰ���Ӧ��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ��
2NH3(g)+92.4 kJ/mol673K��30MPa�£������ϳɰ���Ӧ��n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ����ͼ��ʾ��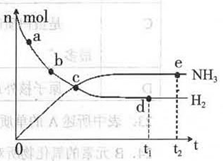
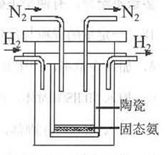
 N2(g)��CO2(g)��2H2O(g) ��H��a kJ/mol
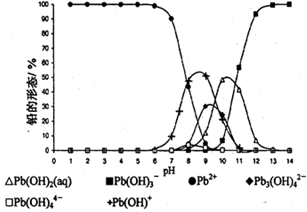
N2(g)��CO2(g)��2H2O(g) ��H��a kJ/mol Pb(s) + CO2(g) ��H���÷�Ӧ��ƽ�ⳣ���Ķ���ֵ���¶ȵĹ�ϵ���±�
Pb(s) + CO2(g) ��H���÷�Ӧ��ƽ�ⳣ���Ķ���ֵ���¶ȵĹ�ϵ���±�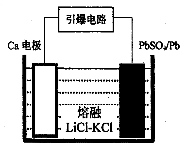
 CH3OH(g)+H2O(g) ��H=��49.0kJ/mol
CH3OH(g)+H2O(g) ��H=��49.0kJ/mol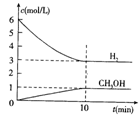
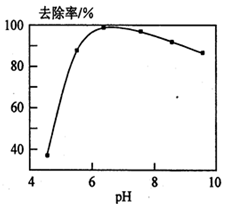
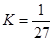 ��CO2��H2��ת�������
��CO2��H2��ת�������