题目内容
18.用化学方程式填空氢氧化钠溶液与硫酸铁溶液反应Fe2(SO4)3+6NaOH=2Fe(OH)3↓+3Na2SO4;
实验室制二氧化碳的原理2HCl+CaCO3=CaCl2+H20+CO2↑;
用高锰酸钾制氧气2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
氢氧化钡和硫酸钠溶液混合Na2SO4+Ba(OH)2=BaSO4↓+2NaOH.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
硫酸铁与氢氧化钠反应生成氢氧化铁红褐色沉淀和硫酸钠;根据实验室石灰石和盐酸反应的原理进行分析;高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,硫酸钠与氢氧化钡反应生成硫酸钡沉淀和氢氧化钠.
解答 解:硫酸铁与氢氧化钠反应生成氢氧化铁沉淀和硫酸钠,其化学方程式为:Fe2(SO4)3+6NaOH=2Fe(OH)3↓+3Na2SO4;
实验室制二氧化碳,用碳酸钙和盐酸反应:2HCl+CaCO3=CaCl2+H20+CO2↑,生成氯化钙、水和二氧化碳;
高锰酸钾在加热条件下反应生成锰酸钾、二氧化锰和氧气,该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
硫酸钠与氢氧化钡反应生成硫酸钡白色沉淀和氢氧化钠,化学方程式为:Na2SO4+Ba(OH)2=BaSO4↓+2NaOH,
故答案为:Fe2(SO4)3+6NaOH=2Fe(OH)3↓+3Na2SO4;2HCl+CaCO3=CaCl2+H20+CO2↑;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;Na2SO4+Ba(OH)2=BaSO4↓+2NaOH.
点评 本题考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等,在解此类题时,首先根据题中的叙述找出反应物、生成物,然后依据方程式的书写规则进行书写,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列各组物质中,具有相同酸根的一组是( )
| A. | K2SO4、Na2SO3 | B. | K2MnO4、NaMnO4 | C. | CaCl2、NaCl | D. | NaCl、KClO3 |
13.下列反应物到生成物的转化不能直接实现的是( )
| A. | Ba(NO3)2─→BaSO4 | B. | H2SO4─→HCl | C. | CuO─→Cu(OH)2 | D. | Ba(OH)2─→Fe(OH)3 |
10.元素周期表是学习和研究化学的重要工具.请根据下表(元素周期表的部分内容)回答有关问题:
(1)请从上表中查出关于硼元素的一条信息:硼元素的相对原子量为10.81.
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的电子层数 相同.
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题:
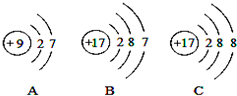
①A、B、C中属于同种元素的粒子是B和C;
②A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥIA | VIIA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)表中3至10号元素位于第二周期,11至18号元素位于第三周期,分析其规律可知,每一周期元素原子的电子层数 相同.
(3)第11号元素与第17号元素组成的化合物是NaCl,构成该物质的微粒是离子(选填“分子”、“原子”或“离子”).
(4)如图A、B、C是三种粒子的结构示意图.试回答下列问题:

①A、B、C中属于同种元素的粒子是B和C;
②A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质.
7.下列各组物质的标准燃烧热相等的是( )
| A. | 碳和一氧化碳 | B. | 1mol碳和2mol碳 | ||
| C. | 1mol乙炔和2mol碳 | D. | 淀粉和纤维素 |
 .
.