题目内容
(4分)
在密闭容器中,将2.0 mol CO与10mol H2O混合加热到800℃,达到下列平衡:CO(g)+H2O(g)
 CO2(g)+H2(g) K=1.0,则CO的转化率为________
CO2(g)+H2(g) K=1.0,则CO的转化率为________
在800℃,若上述反应体系中各物质的浓度分别为c(CO)=2.0mol•L-1,c(H2O)=6.0mol•L-1,c(CO2)=3.0mol•L-1,c(H2)= 4.5mol•L-1,则此时该反应向_________ 方向移动。
【答案】
83.3% 逆反应
【解析】考查可逆反应的有关计算。设CO的转化率是X,容器容积是1L,则
CO(g)+H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)
起始量(mol) 2 10 0 0
转化量(mol) 2x 2x 2x 2x
平衡量(mol) 2-2x 10-2x 2x 2x
所以根据平衡常数的表达式可知 ,解得x=0.833。
,解得x=0.833。
当体系中c(CO)=2.0mol•L-1,c(H2O)=6.0mol•L-1,c(CO2)=3.0mol•L-1,c(H2)=
4.5mol•L-1时, >1,所以反应向逆反应方向移动。
>1,所以反应向逆反应方向移动。

练习册系列答案
 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
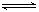 CO2(g)+H2(g) K=1.0,则CO的转化率为________
CO2(g)+H2(g) K=1.0,则CO的转化率为________