题目内容
5.大家知道:Cu+H2SO4(稀)=CuSO4+H2↑通常不能反应.请回答:(1)试说明此反应在一般情况下不能发生反应的原因是铜在金属活动顺序表中排在H元素后,不与稀H2SO4反应.
(2)根据你所学过的知识,设法使其中的反应能发生,具体的方法是用铜作阳极,C棒作阴极,稀H2SO4作电解液,加电源形成电解池; 反应原理是:阳极Cu-2e-=Cu2+阴极2H++2e-=H2↑.
分析 (1)Cu+H2SO4(稀)=CuSO4+H2↑通常不能反应,原因为铜在金属活动顺序表中排在H元素后,不能置换出氢;
(2)要实现Cu+H2SO4(稀)═CuSO4+H2↑,应形成电解池反应,铜为阳极,碳为阴极,阳极发生Cu-2e-=Cu2+,阴极发生2H++2e-=H2↑.
解答 解:(1)Cu+H2SO4(稀)=CuSO4+H2↑通常不能反应,原因为铜在金属活动顺序表中排在H元素后,不能置换出氢,故答案为:铜在金属活动顺序表中排在H元素后,不与稀H2SO4反应;
(2)要实现Cu+H2SO4(稀)═CuSO4+H2↑,应形成电解池反应,铜为阳极,碳为阴极,阳极发生Cu-2e-=Cu2+,阴极发生2H++2e-=H2↑,则可发生Cu+H2SO4(稀)$\frac{\underline{\;通电\;}}{\;}$CuSO4+H2↑,故答案为:用铜作阳极,C棒作阴极,稀H2SO4作电解液,加电源形成电解池;Cu-2e-=Cu2+;2H++2e-=H2↑.
点评 本题考查了电解池原理,侧重于电解池装置的设计,难度不大.

练习册系列答案
相关题目
15.下列离子方程式中,错误的是( )
| A. | 铜丝与硝酸银溶液反应:Cu+Ag+=Cu2++Ag | |
| B. | 氧化铝与稀盐酸混合:Al2O3+6H+=2Al3++3H2O | |
| C. | 稀盐酸与氢氧化钠溶液混合:H++OH-=H2O | |
| D. | 氯气与氢氧化钠溶液反应:Cl2+2OH-=ClO-+Cl-+H2O |
16.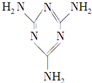 三聚氰胺(结构简式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )
三聚氰胺(结构简式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )
 三聚氰胺(结构简式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )
三聚氰胺(结构简式如图所示)是一种重要的化工原料,可用于阻燃剂、水泥减水剂和高分子合成等领域.一些不法分子却往牛奶中加入三聚氰胺,以提高奶制品的含氮量.下列说法正确的是( )| A. | 三聚氰胺是一种蛋白质 | B. | 三聚氰胺不是高分子化合物 | ||
| C. | 三聚氰胺分子中含有碳碳双键 | D. | 三聚氰胺的分子式为C3H6N6 |
13.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | MgCl2晶体、食盐溶液 | B. | Na2O、干冰 | ||
| C. | 熔融的KOH、液态汞 | D. | 醋酸、氨水 |
10.连二亚硫酸钠(Na2S2O4)是重要的化工原料,该物质在潮湿的空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4═Na2S2O3+X+SO2↑.下列说法不正确的是( )
| A. | X的化学式为Na2SO4 | B. | SO2污染空气 | ||
| C. | Na2S2O3中S的化合价为+2 | D. | Na2S2O4要在干燥阴凉处密闭保存 |
14.在3个温度、容积相同的1L密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得一分钟后反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)??2NH3(g)△H=-92.4kJ•mol-1]:
(1)由以上数据,甲、乙、丙达平衡时,N2的浓度大小关系为甲=乙<丙,从反应开始到达到平衡,甲中以H2表示的反应速率是0.75 mol/(L•min).
(2)该温度下,丙中反应2NH3?N2+3H2的平衡常数是34.17.
(3)a+b=92.4(填“<”、“>”或“=”,下同);α1+α3<1.
(4)若要使甲重新达平衡后$\frac{c(N{H}_{3})}{c({N}_{2})}$比值变小,其他条件可采用BC.
A.使用催化剂 B.增大氮气浓度C.升高温度 D.缩小容器体积.
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
| NH3的浓度(mol•L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | a1=25% | α2 | α3 |
(2)该温度下,丙中反应2NH3?N2+3H2的平衡常数是34.17.
(3)a+b=92.4(填“<”、“>”或“=”,下同);α1+α3<1.
(4)若要使甲重新达平衡后$\frac{c(N{H}_{3})}{c({N}_{2})}$比值变小,其他条件可采用BC.
A.使用催化剂 B.增大氮气浓度C.升高温度 D.缩小容器体积.
