题目内容
【题目】用石墨电极完成下列电解实验。
实验一 | 实验二 | |
装置 |
|
|
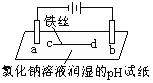
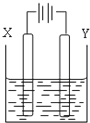
现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生;…… |
下列对实验现象的解释或推测不合理的是( )
A.a、d处:2H2O+2e-=H2↑+2OH-
B.b处:2Cl--2e-=Cl2↑
C.根据实验一的原理,实验二中m处能析出铜
D.n处发生了反应:2H++2e-=H2 ↑
【答案】B
【解析】
试题分析:A.d处试纸变蓝,为阴极,生成OH-,电极方程式为2H2O+2e-═H2↑+2OH-,故A正确;B.b处变红,局部褪色,是因为Cl2+H2O=HCl+HClO,HCl的酸性使溶液变红,HClO的漂白性使局部褪色,故B错误;C.实验一中ac形成电解池,db形成电解池,所以实验二中也相当于形成三个电解池,一个球两面为不同的两极,左边铜珠的左侧为阳极,发生的电极反应为Cu-2e-=Cu2+,右侧(即位置m处)为阴极,发生的电极反应为Cu2++2e-=Cu,同样右边铜珠的左侧为阳极,右侧(即位置n处)为阴极,因此m处能析出铜的说法正确,故C正确;D.根据C的分析,n处为阴极,发生了反应:2H++2e-=H2 ↑,故D正确;故选B。

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目