题目内容
 (1)向蓝色石蕊试纸上滴加几滴饱和氯水,发现试纸先变红后变白.要确证使石蕊褪色的物质是次氯酸,还必须要做的实验是
(1)向蓝色石蕊试纸上滴加几滴饱和氯水,发现试纸先变红后变白.要确证使石蕊褪色的物质是次氯酸,还必须要做的实验是a.干燥的氯气能否使试纸变白b.水能否使试纸变白c盐酸能否使试纸变白
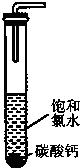
(2)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.如图所示在试管中加入过量的块状碳酸钙.再加入约20ml饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去:过滤,将滤液滴在蓝色石蕊试纸上发现其漂白性比饱和氯水的更强:已知饱和氨水中存在Cl2+H2O?H++Cl-+HClO.反应后所得的溶液漂白性增强的原因是
(3)碳酸钙与氯水反应生成的含钙的化合物除氯化钙外,有人提出如下猜想
a.含次氯酸钙b.含碳酸氢钙c.含次氯酸钙和碳酸氢钙.
有人认为不可能含有次氯酸钙.他的理由可能是
①第一份与澄清石灰水混合,立即产生大量白色沉淀:此实验
②第二份与稀盐酸混合,立即产生大量无色气体:
③将第三份加热,看到溶液变浑浊且有大量无色气体产生.反应的化学方程式为
④除上述实验外,你能设计的确证碳酸氢钙存在的实验方案是
分析:(1)氯水中含有氯气、盐酸、次氯酸等成分;
(2)盐酸酸性比碳酸强,但次氯酸的酸性比碳酸弱;
(3)因次氯酸的酸性比碳酸弱,则次氯酸不与碳酸钙反应,如盐酸不足,可呈生成碳酸氢钙,根据碳酸氢钙的性质设计实验方案.
(2)盐酸酸性比碳酸强,但次氯酸的酸性比碳酸弱;
(3)因次氯酸的酸性比碳酸弱,则次氯酸不与碳酸钙反应,如盐酸不足,可呈生成碳酸氢钙,根据碳酸氢钙的性质设计实验方案.
解答:解:(1)氯气和水反应生成盐酸和次氯酸,要证明次氯酸具有漂白性,应首先排除盐酸的干扰,可价盐酸观察是否褪色,氯水中含有氯气,为排除氯气的干扰,可用干燥的氯气通入试纸,观察试纸是否褪色,故答案为:a、c;
(2)盐酸酸性比碳酸强,但次氯酸的酸性比碳酸弱,加入碳酸钙,发生CaCO3+2H+=Ca2++H2O+CO2↑,使氢离子浓度降低,平衡向正反应方向移动,次氯酸浓度增大,
故答案为:碳酸钙和氢离子反应使其浓度降低,平衡向正反应方向移动,次氯酸浓度增大;
(3)因次氯酸的酸性比碳酸弱,则次氯酸不与碳酸钙反应,则不可能存在次氯酸钙,第一份与澄清石灰水混合,立即产生大量白色沉淀,可说明含有碳酸氢钙,因碳酸氢钙可与石灰水反应生成白色碳酸钙沉淀,将第三份加热,看到溶液变浑浊且有大量无色气体产生,说明含有碳酸氢钙,反应的方程式为Ca(HCO3)2
CaCO3↓+H2O+CO2↑,要证明碳酸氢钙的存在,也可加入氢氧化钠溶液,如观察到有白色沉淀生成,可也证明含有碳酸氢钙,
故答案为:因次氯酸的酸性比碳酸弱,则次氯酸不与碳酸钙反应;能;因碳酸氢钙可与石灰水反应生成白色碳酸钙沉淀;Ca(HCO3)2
CaCO3↓+H2O+CO2↑;向滤液中加入少量氢氧化钠溶液,若有白色沉淀生成,证明含有碳酸氢钙.
(2)盐酸酸性比碳酸强,但次氯酸的酸性比碳酸弱,加入碳酸钙,发生CaCO3+2H+=Ca2++H2O+CO2↑,使氢离子浓度降低,平衡向正反应方向移动,次氯酸浓度增大,
故答案为:碳酸钙和氢离子反应使其浓度降低,平衡向正反应方向移动,次氯酸浓度增大;
(3)因次氯酸的酸性比碳酸弱,则次氯酸不与碳酸钙反应,则不可能存在次氯酸钙,第一份与澄清石灰水混合,立即产生大量白色沉淀,可说明含有碳酸氢钙,因碳酸氢钙可与石灰水反应生成白色碳酸钙沉淀,将第三份加热,看到溶液变浑浊且有大量无色气体产生,说明含有碳酸氢钙,反应的方程式为Ca(HCO3)2
| ||
故答案为:因次氯酸的酸性比碳酸弱,则次氯酸不与碳酸钙反应;能;因碳酸氢钙可与石灰水反应生成白色碳酸钙沉淀;Ca(HCO3)2
| ||
点评:本题考查性质的实验方案的设计,侧重于学生的分析能力和实验能力的考查,为高考常见题型和高频考点,注意把握实验的原理、步骤和实验方法,根据物质的性质解答该题,难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
 H++C1-+HClO.反应后所得的溶液漂白性增强的原因是
(用化学平衡移动原理解释)。
H++C1-+HClO.反应后所得的溶液漂白性增强的原因是
(用化学平衡移动原理解释)。