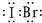题目内容
(1)新制氯水呈 色,说明溶液中有 分子存在;向氯水中加入锌粉,立即有 生成,说明氯水中含有 离子;
(2)蓝色石蕊试纸遇到氯水后,先变 ,接着 ,这是因为 ;
(3)氯水经光照后放出气体,该反应的化学方程式为 .
(2)蓝色石蕊试纸遇到氯水后,先变
(3)氯水经光照后放出气体,该反应的化学方程式为
分析:(1)新制氯水含Cl2、盐酸、HClO、H2O等物物质,具有酸的性质;
(2)HClO具有漂白性;
(3)HClO不稳定,见光易分解.
(2)HClO具有漂白性;
(3)HClO不稳定,见光易分解.
解答:解:(1)新制氯水含Cl2、盐酸、HClO、H2O等物物质,含Cl2分子则氯水呈黄绿色,含酸电离的H+,则加入锌粉,立即生成氢气,故答案为:黄绿;Cl2;气体;H+;
(2)氯水含盐酸和次氯酸,则蓝色石蕊试纸遇到氯水后先变红后褪色,是因氯水具有酸性和漂白性,故答案为:红;褪色;既有酸性又有漂白性;
(3)HClO不稳定,见光易分解,该反应为2HClO
2HCl+O2↑,故答案为:2HClO
2HCl+O2↑.
(2)氯水含盐酸和次氯酸,则蓝色石蕊试纸遇到氯水后先变红后褪色,是因氯水具有酸性和漂白性,故答案为:红;褪色;既有酸性又有漂白性;
(3)HClO不稳定,见光易分解,该反应为2HClO
| ||
| ||
点评:本题考查氯水的成分以及次氯酸性质,把握氯水中的三种分子四种离子的性质及HClO的漂白性和不稳定性为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目