题目内容
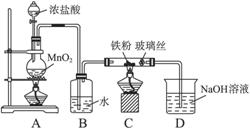
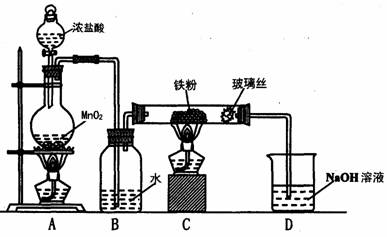
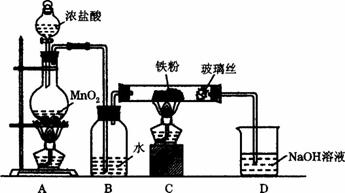
现有一份含有FeCl3和FeCl2的固体混合物,某化学兴趣小组为测定各成分的含量进行如下两个实验:
实验1:
①称取一定质量的样品,将样品溶解;②向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;③将沉淀过滤、洗涤、干燥得到白色固体28.7g.
实验2:
①称取与实验1中相同质量的样品,溶解;②向溶解后的溶液中通入足量的Cl2;③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀;④将沉淀过滤、洗涤后,加热灼烧到质量不再减少,得到固体Fe2O36.40g.
根据实验回答下列问题:
(1)溶解过程中所用到的玻璃仪器有______.
(2)实验室保存FeCl2溶液时通常会向其中加入少量的铁粉,其作用是(用方程式表示)______.
(3)用化学方程式表示实验2的步骤②中通入足量Cl2的反应:______.
(4)用容量瓶配制实验所用的NaOH溶液,下列情况会使所配制溶液浓度偏高的是(填序号)______.
A.未冷却溶液直接转移
B.没用少量蒸馏水洗涤烧杯和玻璃棒2-3次并转入容量瓶
C.加蒸馏水时,不慎超过了刻度线
D.砝码上沾有杂质
E.容量瓶使用前内壁沾有水珠
(5)检验实验2的步骤④中沉淀洗涤干净的方法是______.
(6)该小组取来的样品中含有FeCl2的质量为______g.
解:(1)溶解所用到的仪器为:烧杯、玻璃棒;FeCl2易被空气中的氧气氧化成FeCl3,向溶液中加入少量铁粉,使被氧气氧化产生的FeCl3重新转化为FeCl2;故答案为:烧杯、玻璃棒; 防止溶液里的Fe2+被氧化;
(2)Cl2将FeCl2氧化生成FeCl3:Cl2+2FeCl2=2FeCl3,故答案为:Cl2+2FeCl2=2FeCl3;
(3)A.未冷却溶液直接转移,会导致溶液体积偏小,溶液浓度偏高;
B.没用少量蒸馏水洗涤烧杯和玻璃棒2-3次并转入容量瓶,会导致溶质的质量偏小,溶液浓度偏低;
C.加蒸馏水时,不慎超过了刻度线,导致溶液体积偏大,所以溶液浓度偏低.
D.砝码上沾有杂质,会导致溶质的质量偏大,溶液浓度偏高;
E.容量瓶使用前内壁沾有水珠,不影响溶质的物质的量和对溶液的体积,对溶液浓度无影响;
故选:AC.
(4)因为氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,所以如果最后一次的洗涤液仍然有氯化钠,加入硝酸银溶液就会出现沉淀,反之,说明溶液中没有氯化钠,故答案为:取少量最后一次的洗涤液于试管中,向试管中溶液加适量AgNO3溶液,如未出现白色沉淀说明已洗净;
(5)FeCl3和FeCl2的物质的量分别为amol,bmol;
则有3amol+2bmol= =0.2mol(氯守恒)
=0.2mol(氯守恒)
amol+bmol=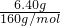 ×2=0.08mol(铁守恒)
×2=0.08mol(铁守恒)
解得:a=0.04,b=0.04
FeCl2的质量为0.04mol×127g/mol=5.08g,故答案为:5.08.
分析:(1)根据溶解所用到的仪器为:烧杯、玻璃棒;根据FeCl2易被空气中的氧气氧化成FeCl3,向溶液中加入少量铁粉,使被氧气氧化产生的FeCl3重新转化为FeCl2;
(2)Cl2将FeCl2氧化生成FeCl3;
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=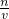 分析判断;
分析判断;
(4)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠即可;
(5)设FeCl3和FeCl2的物质的量分别为amol,bmol,建立方程式组来求解.
点评:本题主要考查了化学实验以及化学计算,难度不大,在计算时抓住元素守恒.
(2)Cl2将FeCl2氧化生成FeCl3:Cl2+2FeCl2=2FeCl3,故答案为:Cl2+2FeCl2=2FeCl3;
(3)A.未冷却溶液直接转移,会导致溶液体积偏小,溶液浓度偏高;
B.没用少量蒸馏水洗涤烧杯和玻璃棒2-3次并转入容量瓶,会导致溶质的质量偏小,溶液浓度偏低;
C.加蒸馏水时,不慎超过了刻度线,导致溶液体积偏大,所以溶液浓度偏低.
D.砝码上沾有杂质,会导致溶质的质量偏大,溶液浓度偏高;
E.容量瓶使用前内壁沾有水珠,不影响溶质的物质的量和对溶液的体积,对溶液浓度无影响;
故选:AC.
(4)因为氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,所以如果最后一次的洗涤液仍然有氯化钠,加入硝酸银溶液就会出现沉淀,反之,说明溶液中没有氯化钠,故答案为:取少量最后一次的洗涤液于试管中,向试管中溶液加适量AgNO3溶液,如未出现白色沉淀说明已洗净;
(5)FeCl3和FeCl2的物质的量分别为amol,bmol;
则有3amol+2bmol=
 =0.2mol(氯守恒)
=0.2mol(氯守恒) amol+bmol=
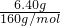 ×2=0.08mol(铁守恒)
×2=0.08mol(铁守恒)解得:a=0.04,b=0.04
FeCl2的质量为0.04mol×127g/mol=5.08g,故答案为:5.08.
分析:(1)根据溶解所用到的仪器为:烧杯、玻璃棒;根据FeCl2易被空气中的氧气氧化成FeCl3,向溶液中加入少量铁粉,使被氧气氧化产生的FeCl3重新转化为FeCl2;
(2)Cl2将FeCl2氧化生成FeCl3;
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
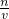 分析判断;
分析判断;(4)根据氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠即可;
(5)设FeCl3和FeCl2的物质的量分别为amol,bmol,建立方程式组来求解.
点评:本题主要考查了化学实验以及化学计算,难度不大,在计算时抓住元素守恒.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目