题目内容
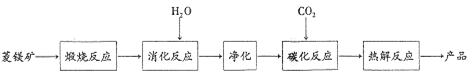
【题目】用海水可同时生产氯化钠和金属镁或镁的化合物,其流程如下图所示:

(1)在实验室中由粗盐“重结晶”的操作包括溶解、过滤、蒸发、_________(填操作方法)、洗涤等步骤;有关其中“蒸发”步骤的叙述错误的是____________。
a. 蒸发的目的是得到热饱和溶液 b. 蒸发的目的是析出晶体
c. 应用余热蒸干溶液 d. 应蒸发至有较多晶体析出时为止
(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度曲线,蒸发的目的是_________。

a. 得到热饱和溶液 b. 析出晶体
(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:__________。
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____________________________________。
(5)MgCl2可电解制Mg,MgO则是重要的耐火材料。在550℃时,MgCl2·6H2O会分解生成MgO、MgCl2、HCl和H2O,若不补充其它原料,使一定量的MgCl2·6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则a∶b为______________(取整数值)。
【答案】 过滤 ac a MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑ 用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠(答“焰色反应”也可) 3∶1(或3)
Mg(OH)Cl+HCl↑+5H2O↑ 用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠(答“焰色反应”也可) 3∶1(或3)
【解析】贝壳中含有CaCO3,煅烧贝壳得到CaO,发生的反应为CaCO3![]() CO2↑+CaO,CaO和水发生反应CaO+H2O=Ca(OH)2得到石灰乳;海水通过蒸发得到粗盐和母液,粗盐通过溶解、重结晶得到精盐;将石灰乳加入母液中发生反应Ca(OH)2+MgCl2=Mg(OH)2+CaCl2,将Mg(OH)2加入稀盐酸中,发生反应 Mg(OH)2+2HCl=MgCl2+2H2O,然后浓缩得到MgCl2·6H2O,将MgCl2·6H2O在HCl氛围中加热得到MgCl2,则
CO2↑+CaO,CaO和水发生反应CaO+H2O=Ca(OH)2得到石灰乳;海水通过蒸发得到粗盐和母液,粗盐通过溶解、重结晶得到精盐;将石灰乳加入母液中发生反应Ca(OH)2+MgCl2=Mg(OH)2+CaCl2,将Mg(OH)2加入稀盐酸中,发生反应 Mg(OH)2+2HCl=MgCl2+2H2O,然后浓缩得到MgCl2·6H2O,将MgCl2·6H2O在HCl氛围中加热得到MgCl2,则
(1)在实验室中由粗盐“重结晶”制精盐的操作包括溶解、蒸发、过滤、洗涤等步骤;a.氯化钠的溶解度受温度影响不大,所以蒸发的目的是析出晶体,a错误;b.根据a知,蒸发的目的是析出晶体,b正确;c.因为溶液中含有大量杂质,所以不能蒸干溶液,c错误;d.应蒸发至有较多晶体析出时为止,因为溶液中含有大量杂质,所以不能蒸干溶液,否则得到的仍然是混合物,d正确;答案选ac;(2)由MgCl2溶液得到MgCl2·6H2O也需要蒸发,根据溶解度如图2曲线,蒸发的目的是得到热的饱和溶液,然后冷却得到MgCl2·6H2O,答案选a;(3)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl,根据反应物、生成物及反应条件知,该反应的化学方程式:MgCl2·6H2O![]() Mg(OH)Cl+HCl↑+5H2O↑;(4)根据焰色反应检验氯化钠,即用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠;(5)假设是1molMgCl26H2O发生反应,根据Mg原子守恒得a+b=1mol①,盐酸的质量=1mol×203g/mol-amol×40g/mol-bmol×95g/mol=(203-40a-95b)g,HCl的物质的量=(20340a95b)g×36.5%/36.5g/mol=[(203-40a-95b)×1%]mol,根据Cl原子守恒得2mol=[2b+0.01×(203-40a-95b)]mol②,联立①②得a=108/145、b=37/145,所以a:b=108/145:37/145=3:1。
Mg(OH)Cl+HCl↑+5H2O↑;(4)根据焰色反应检验氯化钠,即用铂丝蘸取少量固体,置于酒精灯火焰上灼烧,若无黄色产生,则证明所得无水氯化镁晶体中不含氧化钠;(5)假设是1molMgCl26H2O发生反应,根据Mg原子守恒得a+b=1mol①,盐酸的质量=1mol×203g/mol-amol×40g/mol-bmol×95g/mol=(203-40a-95b)g,HCl的物质的量=(20340a95b)g×36.5%/36.5g/mol=[(203-40a-95b)×1%]mol,根据Cl原子守恒得2mol=[2b+0.01×(203-40a-95b)]mol②,联立①②得a=108/145、b=37/145,所以a:b=108/145:37/145=3:1。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案