题目内容
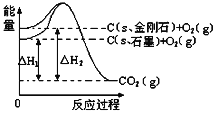
【题目】某小组探究元素周期律,甲根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的研究;乙根据置换反应的规律,利用下图装置完成O元素的非金属性比S强的研究。回答:
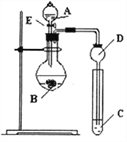
(1)图中A装置名称是______________。
(2)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3 溶液 ⑤SiO2
试剂A与C分别为_________(填序号);试管中发生反应的离子方程式为_______________.有同学认为此实验不能说明N、C、S的非金属性强弱,你认为原因是_________________
(3)乙同学设计的实验所用到试剂A为________;如果C试剂为硫化氢的水溶液,则试管中可以观察到的现象为_______________
【答案】 分液漏斗 ①④ CO2+H2O+SiO32-=H2SiO3+CO32- HNO3有挥发性也会和硅酸钠反应生成硅酸 双氧水 有淡黄色浑浊出现
【解析】(1)由仪器的结构特征,可知A为分液漏斗;
(2)探究元素非金属性,由图可知应是利用最高价含氧酸的酸性强弱比较,所以A中试剂为稀硝酸,B中为碳酸钙,C中为Na2SiO3溶液;试管中为Na2SiO3溶液中通CO2生成硅酸白色沉淀,发生反应的离子方程式为CO2+H2O+SiO32-=H2SiO3+CO32-;通入试管中的CO2气体中混有挥发性的硝酸,硝酸也能与硅酸钠溶液反应生成硅酸,无法确定CO2是否与与硅酸钠溶液反应,即不能说明N、C、S的非金属性强弱;
(3)乙同学欲证明氧的非金属性比硫强,需要通过实验证明氧气能制取硫单质来实现,则试剂A为H2O2,在MnO2催化作用下分解生成氧气;生成的氧气通入盛有硫化氢的水溶液中,有淡黄色浑浊出现,说明有硫生成。