题目内容
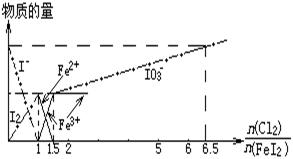
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。
据此得出的下列结论中错误的是

据此得出的下列结论中错误的是
| A.I-、Fe2+、I2的还原性和Cl2、Fe3+、I2的氧化性都依次减小 |
| B.当n(Cl2)/n(FeI2)==1.2时,离子方程式为2Fe2++10I-+6Cl2==5I2+2Fe3++12Cl- |
| C.当n(Cl2)/n(FeI2)==6.5时,溶液中n(Cl-)/n(IO3-)==6.5 |
| D.若溶液体积不变,溶液的pH始终不变 |
D
由图示可知随Cl2、FeI2的物质的量比增加,当Cl2、FeI2比值小于1仅发生的反应为2I-+Cl2==I2+2Cl-,当Cl2、FeI2比值在1和1.5之间时,2I-+Cl2==I2+2Cl-完全反应,2Fe2++Cl2==2Fe3++2Cl-部分反应,当Cl2、FeI2比值在1.5和6.5之间时,仅发生反应I2+5Cl2+6H2O=2HIO3+10HCl。由于碘酸和盐酸均为强酸,最终溶液呈强酸性溶液的pH减小。

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
 HSO
HSO 稀溶液至刚好沉淀完全:
稀溶液至刚好沉淀完全: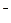 +NH
+NH +H
+H +SO
+SO ====BaSO
====BaSO ·H
·H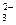 +CO
+CO Ag2S↓
Ag2S↓