题目内容
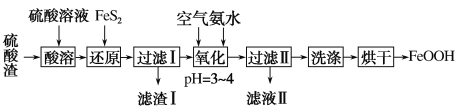
【题目】利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如下:
(1)“酸溶”时,Fe2O3与硫酸反应的离子方程式为___________________。
(2)滤渣I的主要成分是FeS2、S和___________(填化学式);Fe3+被FeS2还原的离子方程式为_______________。
(3)“氧化”中,生成FeOOH的离子方程式为_______________。
【答案】Fe2O3+6H+===2Fe3++3H2O SiO2 2Fe3++FeS2===3Fe2++2S 4Fe2++8NH3·H2O+O2===4FeOOH↓+8NH![]() +2H2O
+2H2O
【解析】
硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)加硫酸溶解,金属氧化物转化为金属阳离子,二氧化硅不溶,再加FeS2把铁离子还原为Fe2+,同时生成S沉淀,过滤,滤渣含有二氧化硅和S以及过量的FeS2,滤液中含有Fe2+和Al3+,滤液中通入空气氧化,同时用氨水调节pH生成FeOOH沉淀,过滤、洗涤、烘干,得到纯净的FeOOH,以此解答该题。
(1)酸溶时,Fe2O3与硫酸生成硫酸铁和水,离子方程式为Fe2O3+6H+===2Fe3++3H2O;
(2)滤渣I的主要成分是不溶于硫酸的SiO2和S以及过量的FeS2;Fe3+被FeS2还原成Fe2+,硫元素被氧化成S单质,根据电子守恒和元素守恒可得离子方程式为2Fe3++FeS2===3Fe2++2S;
(3)根据流程可知反应物有Fe2+、O2和NH3·H2O,产物有FeOOH,氧气做氧化剂将2价铁氧化成3价铁,结合电子守恒和元素守恒可得离子方程式为4Fe2++8NH3·H2O+O2===4FeOOH↓+8NH![]() +2H2O。
+2H2O。