题目内容
【题目】甲元素原子的![]() 能层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
能层上只有一个空原子轨道;乙元素原子的核电荷数为33。根据甲、乙两元素的信息,回答有关问题:
(1)甲的元素符号是______;其电子排布图为______。
(2)乙元素原子的最外层电子排布式为______,其在元素周期表中的位置是______。
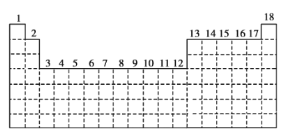
(3)甲属于______区元素,乙属于______区元素。
【答案】![]()
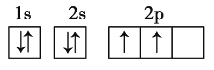
![]() 第四周期第ⅤA族 p p
第四周期第ⅤA族 p p
【解析】
(1)甲元素原子的![]() 能层上只有一个空原子轨道,则L能层的2p能级含有一个空轨道,则甲核外电子数是6,为C元素,根据构造原理书写其核外电子排布式;
能层上只有一个空原子轨道,则L能层的2p能级含有一个空轨道,则甲核外电子数是6,为C元素,根据构造原理书写其核外电子排布式;
(2)原子的核电荷数为33,则乙是As元素,其4s、4p电子为其外围电子,根据能量最低原理书写其外围电子排布式,主族元素的电子层数与其周期数相等、最外层电子数与其族序数相等,确定周期和族;
(3)根据最后排入的电子判断该元素所属区域;
(1)甲元素原子在第二能层上只有一个空轨道,则L能层的2p能级含有一个空轨道,则甲核外电子数是6,为C元素,根据构造原理知其核外电子排布式1s22s22p2,核外电子排布图为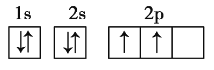 ;
;
(2)乙原子的核电荷数为33,则乙是As元素,其4s、4p电子为其外围电子,根据能量最低原理知其外围电子排布式4s24p3,主族元素的电子层数与其周期数相等、最外层电子数与其族序数相等,所以As元素位于第四周期第VA族;
(3)甲元素最后排入的电子是p电子,所以甲属于p区, As最后排入的电子是p电子,所以属于p区。

练习册系列答案
相关题目