题目内容
【题目】已知常温下,HCOOH(甲酸)比NH3H2O电离常数大。向10 mL 0.1mol/L HCOOH中滴加同浓度的氨水,有关叙述正确的是( )
A. 滴加过程中水的电离程度始终增大
B. 当加入10 mL NH3H2O时,c(NH4+) > c(HCOO-)
C. 当两者恰好中和时,溶液pH = 7
D. 滴加过程中n(HCOOH)与n(HCOO-)之和保持不变
【答案】D
【解析】
A.HCOOH溶液中水的电离被抑制,向HCOOH溶液中加氨水时,HCOOH浓度逐渐减小,HCOOH对水的抑制作用减弱,水的电离程度逐渐增大,随后生成的HCOONH4的水解反应,也促进水的电离,继续加过量的氨水,氨水电离的OH-使水的电离平衡左移,水的电离程度减小,所以整个过程中水的电离程度先增大后减小,A项错误;
B. 当加入10mL NH3·H2O时,HCOOH+NH3·H2O=HCOONH4+H2O,恰好反应,所得溶液是HCOONH4溶液,溶液中存在水解平衡:HCOO-+H2O![]() HCOOH+OH-,NH4++H2O
HCOOH+OH-,NH4++H2O![]() NH3·H2O+H+,因HCOOH比NH3·H2O电离常数大,NH4+的水解程度比HCOO-大,所以c(NH4+)<c(HCOO-),B项错误;
NH3·H2O+H+,因HCOOH比NH3·H2O电离常数大,NH4+的水解程度比HCOO-大,所以c(NH4+)<c(HCOO-),B项错误;
C. 当两者恰好中和时,HCOOH+NH3·H2O=HCOONH4+H2O,所得溶液是HCOONH4溶液,溶液中存在水解平衡:HCOO-+H2O![]() HCOOH+OH-,NH4++H2O
HCOOH+OH-,NH4++H2O![]() NH3·H2O+H+,因HCOOH比NH3·H2O电离常数大,NH4+的水解程度比HCOO-大,溶液中c(H+)>c(OH-),溶液显酸性,pH<7,C项错误;
NH3·H2O+H+,因HCOOH比NH3·H2O电离常数大,NH4+的水解程度比HCOO-大,溶液中c(H+)>c(OH-),溶液显酸性,pH<7,C项错误;
D.向HCOOH溶液中加氨水,HCOOH的初始物质的量没有变,根据物料守恒,滴加过程中n(HCOOH)+n(HCOO-)=0.01L×0.1mol/L=0.001mol,D项正确;答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
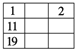
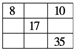
a | b | c | |||||||||||||||
e | f | ||||||||||||||||
试回答下列问题:
(1)写出元素e的基态原子电子排布式________________,其未成对电子数为________。
(2)c在空气中燃烧产物的分子构型为_____,中心原子的杂化形式为______杂化。c能形成一种八元环状形同王冠的单质分子,原子的杂化形式为______杂化。
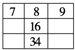
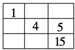
(3)b单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
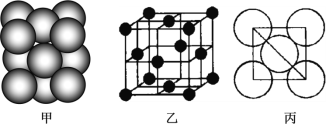
若已知b的原子半径为d厘米,NA代表阿伏加德罗常数,b的相对原子质量为M,请回答:
①晶胞中b原子的配位数为_____,表示原子空间占有率的代数式为_____________。
②该晶体的密度为_____________g/cm3(用含有关字母的代数式表示)。a、f中,与单质b晶体中原子的堆积方式相同的是__________(填元素符号)。