题目内容
(8分)有A、B、C、D四种短周期元素, 它们的原子序数由A到D依次增大, 已知A和B原子有相同的电子层数, 且A的L层电子数是K层电子数的两倍, C燃烧时呈现黄色火焰, C的单质在高温下与B的单质充分反应, 可以得到与D单质颜色相同的淡黄色固态化合物, 试根据以上叙述回答:
(1)元素名称: A B C D
(2)写出AB2的电子式为
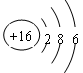
(3)画出D的原子结构示意图 , 用电子式表示化合物 C2D 的形成过程 。
(1)元素名称: A B C D
(2)写出AB2的电子式为
(3)画出D的原子结构示意图 , 用电子式表示化合物 C2D 的形成过程 。
(1)碳氧 钠 硫 (2)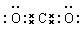 (3)
(3)

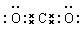 (3)
(3)

考查原子核外电子的排布规律。A的L层电子数是K层电子数的两倍,则A是碳。C燃烧时呈现黄色火焰,所以C是Na。淡黄色固态化合物是过氧化钠,所以B是O,D是S。CO2是由极性键形成的共价化合物,而Na2S是由离子键形成的离子化合物。

练习册系列答案
相关题目
 ,则该微粒一定是氩原子
,则该微粒一定是氩原子